题目内容
【题目】化学实验和化学计算都是化学学习的重要内容.
(一)通过学习,我们已经掌握了一些气体的制备方法,如制取氧气的方法有:
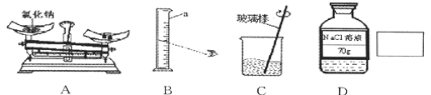
甲.分离液体空气; 乙.加热分解高锰酸钾; 丙.分解过氧化氢; 丁.加热分解氯酸钾等;也初步认识了一些气体的制取和收集装置,例如:

(1)仪器a 的名称是_____.
(2)以上制取氧气的方法中,属于物理方法的是_____;
(3)若用方法丙制取氧气,应选用的装置组合为_____(填字母序号)
(二)在现代生活中,人们越来越注重微量元素的摄取.碘元素对人体有着至关重要的作用.
如图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,请回答下列问题:

(1)食用“碘盐”属于_____;(纯净物或混合物)
(2)根据碘盐的食用方法和贮存指南,可推知碘酸钾的化学性质之一是:_____
(3)碘酸钾(KIO3)中钾元素、碘元素的质量比是_____, 碘酸钾(KIO3)中碘元素的质量分数的计算式是_____.
【答案】集气瓶 甲 BC(BE) 混合物 受热易分解 39:127 ![]() ×100%
×100%
【解析】
(一)(1)仪器a 的名称是:集气瓶;
(2)分离液态空气得到氧气属于物理变化,属于物理方法的有:甲;
(3)如果用双氧水和二氧化锰制氧气就不需要加热,应选用的装置组合为BC(BE);
(二)(1)食用“碘盐”中含有氯化钠、碘酸钾,食用“碘盐”属于混合物;
(2)根据碘盐的食用方法和贮存指南,可推知碘酸钾的化学性质之一是:受热易分解;
(3)碘酸钾(KIO3)中钾元素、碘元素的质量比为39:127;碘酸钾(KIO3)中碘元素的质量分数的计算式是:![]() ×100%。
×100%。

 名校课堂系列答案
名校课堂系列答案【题目】实验室中可以用高锰酸钾、过氧化氢、氯酸钾来制取并收集氧气。根据所学知识回答问题:
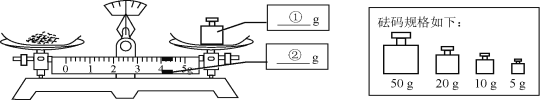
(1)结合下图所提供装置完成下列表格
填写内容 反应物 | 化学反应的符号表达式 | 实验装置(填字母) |
高锰酸钾 | 例: KMnO4 | |
过氧化氢(二氧化锰) | _________ | _______ |
氯酸钾(二氧化锰) | _________ | _______ |
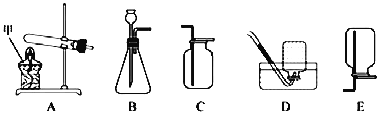
(2)请结合上图回答问题:
①写出甲所指仪器名称:甲_______;
②检查B装置气密性的方法是:向长颈漏斗中加水至末端浸没在水面以下,从导管处向外抽气,若观察到_______,则气密性良好;
③用过氧化氢制氧气的装置与其他两种方法的装置相比具有的优点________(写出一条);
④用如图装置收集O2,验满的方法是_______。

⑤ 实验室用大理石(固体)和稀盐酸(液体)常温下反应制取并收集二氧化碳(CO2能溶于水,其密度大于空气的密度,且不与空气中的成分发生反应),应选用的实验装置为_______。(填字母)
(3)某兴趣小组的同学借助氧气传感器探究微粒的运动,数据处理软件可实时绘出氧气体积分数随时间变化的曲线。收集一塑料瓶氧气进行以下三步实验:第一步 敞口放置;第二步 双手贴在塑料瓶外壁上;第三步 将塑料瓶的瓶口朝下,三步实验中测得氧气的体积分数随时间变化的曲线依次为下图中的MN段、NP段和PQ段。


①能够说明氧分子不断运动的曲线是_______。
A.MN段 B.NP段 C.PQ段
②MN段和NP段相比较,说明______。
③随着实验的进行,传感器测出氧气的体积分数约为____时几乎不再变化。
【题目】秋天正是水中莲藕上市的季节。据说多吃可以使人多长“心眼”而更加聪明。同学们对藕孔中的气体成分进行探究。
(1)检验藕孔气体中是否含有二氧化碳
实验步骤 | 实验现象 | 实验结论及解释 |
A组同学用注射器从藕孔中抽取气体,向所取气体中加入____________ | ____________ | 有二氧化碳,反应的化学方程式为_______________ |
B组同学采用排水法也收集同样体积的气体,重复上述实验,实验现象不如A组明显,其原因是____________。
(2)比较藕孔气体和空气中氧气的含量
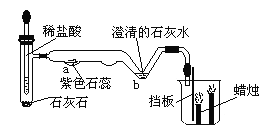
(设计实验)同学们设计如下图所示的方案一和方案二来测定氧气含量。

①实验中红磷应该足量,原因是_____。红磷燃烧的化学方程式为________。
②方案二某些方面优于方案一,下列评价正确的是______。(填序号)
a.方案二测定结果更准确 b.方案二污染小 c.方案二节约药品
(进行实验)同学们按方案二进行实验。按图组装仪器后,应先_______。
(实验现象)流入的水约占瓶容积的1/10。
(实验结论)______。
【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验:
①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ、将3g氯酸钾与1g二氧化锰均匀混合加热
Ⅱ、将xg氯酸钾与1g氧化铜均匀混合加热
在相同温度下,比较两组实验产生氧气的快慢。
Ⅰ反应中文字表达式是____________
Ⅱ中x的值应为______
②乙探究了影响过氧化氢分解速度的某种因素。实验数据记录如下:
过氧化氢的质量 | 过氧化氢的浓度 | 二氧化锰的质量 | 相同时间内产生氧气的体积 | |
Ⅰ | 50g | 1% | 0.1g | 9mL |
Ⅱ | 50g | 2% | 0.1g | 16mL |
Ⅲ | 50g | 4% | 0.1g | 31mL |
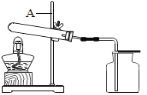
本实验中,测量氧气体积的装置是____________(填编号)
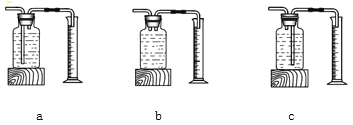
实验结论如下:在相同条件下,_______,过氧化氢分解得越快。