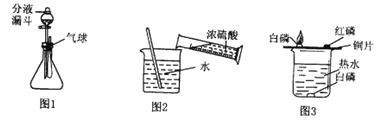题目内容
【题目】用下图装置验证CO2的相关性质。
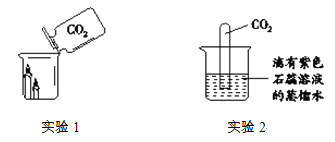
(1)实验1:观察到的实验现象是______。该实验说明CO2具有的性质是______。
(2)实验2:一段时间后,观察到的实验现象是______、______。该反应的化学方程式是______。
【答案】 蜡烛自下而上依次熄灭 相同条件下,CO2的密度比空气大,CO2不支持燃烧;CO2不可以燃烧 试管中液面上升 溶液由紫色变为红色 CO2 + H2O === H2CO3
【解析】(1)根据二氧化碳不燃烧也不支持燃烧且密度比空气大分析解答;(2)根据二氧化碳与水反应生成碳酸分析解答。(1)实验1:观察到的实验现象是蜡烛自下而上依次熄灭;该实验说明CO2具有的性质是相同条件下,CO2的密度比空气大,CO2不支持燃烧;CO2不可以燃烧;(2)实验2:二氧化碳能与水反应生成碳酸(碳酸能使紫色石蕊溶液变红),导致试管内压强降低,在外界气压的作用下试管中液面上升;该反应的化学方程式是CO2 + H2O = H2CO3。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案【题目】(1)经过一年化学学习.你可能已经喜欢上了在实验室做实验的感觉。让我们一起再来做实验吧
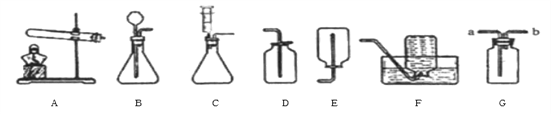
①实验室用装置A制取氧气,若要收集一瓶较纯净的氧气,应选择装置_____(填字母)若用G装置收集氧气,验满方法为_______________;
②通常情况下,乙炔是一种密度比空气略小.且难溶于水的气体。实验室常用块状碳化钙固体和水反应制取乙炔,该反应在常温下进行且非常剧烈。实验室欲制取乙炔,最好选用的装置组合是________(填字母),该发生装置的优点为__________。
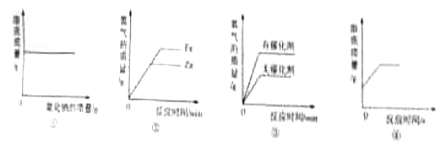
(2)化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸 逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如下图所示。
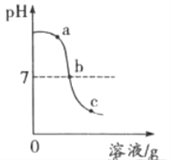
【提出问题】导致溶液pH变化的原因是什么?
【查阅资料】
①溶液的pH是由H+或OH-浓度决定,H+浓度越大,pH越小;OH-浓度越大,pH越大。
②溶液中某种离子浓度非常小时,可忽略不计。
【作出猜想】
猜想Ⅰ:溶液pH变化是因为氢氧化钠溶液被稀释。
猜想Ⅱ:溶液pH变化是因为发生了化学反应。
【进行实验】同学们分成两组分别进行实验。
甲组:同学们将4mL2%的稀硫酸换成__________,逐滴滴加到2mL2%的氢氧化钠溶液中,并测得溶液的pH始终大于7,说明猜想Ⅰ不合理。
乙组:同学们分别取a、b、c三处溶液进行实验。
实验操作 | 实验现象 | 实验分析 |
取适量a处溶液于试管中,加入镁条 | 无气泡产生 | 溶液中几乎不含___(填离子符号) |
取适量b处溶液于试管中,加入紫色石蕊溶液 | _________ | 溶液中几乎不含H+和OH- |
取适量c处溶液于试管中,加入___________ | ___________ | 溶液中几乎不含OH- |
【实验结论】猜想Ⅱ合理。
【知识拓展】从微观角度分析,中和反应的实质是_________。
【题目】实验操作考试考试中为了制取氧气和二氧化碳,实验室提供了以下药品和仪器装置,请回答下列问题:
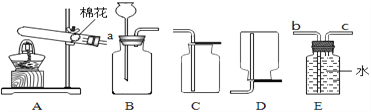
(1)小英同学选择B装置制取氧气,反应的化学方程式为____________,若她选择E装置收集氧气,则将a与________________相连。
(2)小东抽到的实验是制取二氧化碳并检查其性质,他选择的药品是用盐酸和碳酸钙固体反应,若想控制选择的发生装置B的反应速率,他可以将装置中的一种仪器替换为________;他在将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊(装置气密性良好)。
【提出假设】假设一:澄清石灰水已变质:
假设二:气体X中除了有CO2外,还有__________
【实验探究】用下图所示实验探究上述假设是否合理。
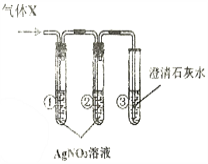
【现象与结论】
实验 | 现象 | 分析与结论 |
一 | 若:试管①中________, 试管②中无明显变化, 试管③中液体变浑浊。 | 试管③中发生反应的化学方程式为_________, 结论:假设二成立。 |
二 | 若:试管①中出现白色沉淀, 试管②中无明显变化, 试管③中无明显变化。 | 试管②中试剂的作用是________, 结论:_______成立。 |
【题目】空气是我们赖以生存的宝贵资源。
(1)空气属于_____(填“纯净物”或“混合物”),其中能供给呼吸的物质是_____。
(2)下表为北京市某监测点监测到的空气质量。依据表格回答问题:

污染项目 | PM2.5 | PM10 | SO2 | CO | NO2 |
污染指数 | 69 | 95 | 9 | 0.8 | 42 |
①首要污染物是______;其中会形成酸雨的是______(填1种即可)。
② 上图为一款新型环保车,可通过360 °旋转的“大炮筒”向四周喷水,从而缓解极端恶劣天气给人带来的不适。分析这款环保车喷水的作用是______。