题目内容
老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
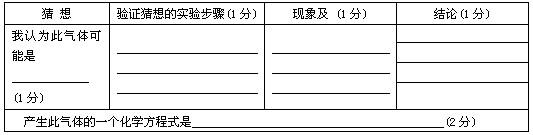
(1)①请你猜想此气体可能是什么物质?如何验证该气体?
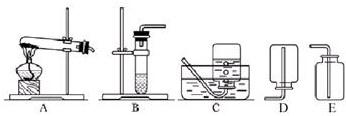
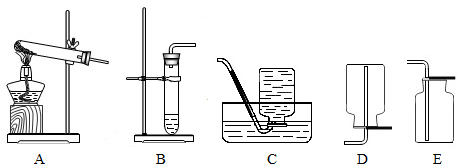
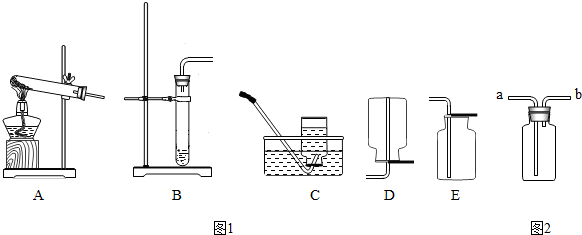
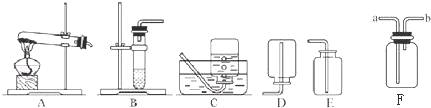
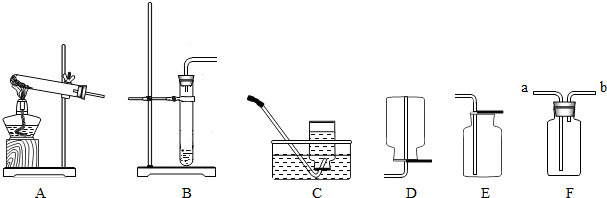
②你想制取该无色气体,发生装置将选取下图中的______(填序号,下同),收集装置选取______;
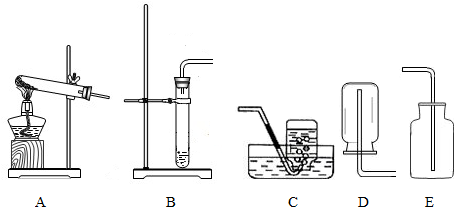
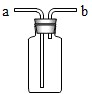
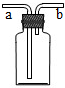
③如果用如图所示装置收集你猜想的气体,你认为气体应从______ 端(填“a”或“b”)通入.
④请你猜想该无色气体还可能是另外一种气体,产生它的其中一个化学方程式是______;收集装置可采用②图中的______.
(2)向50g 8%的氢氧化钠溶液中加入100g的稀盐酸恰好完全反应,此时溶液PH=7.求:所用稀盐酸溶质的质量分数是多少?反应后生成氯化钠溶液溶质的质量分数为多少?
解:(1)①二氧化碳可由固体石灰石与液休稀盐酸在常温下反应制得,因此,可猜想该气体为二氧化碳;可把气体通入澄清石灰水进行检验,石灰水变浑浊可说明气体为二氧化碳;
②由于制取二氧化碳使用块状固体与液体常温下反应制取,因此可选择B装置作为制取气体的发生装置;由于二氧化碳能溶于水且密度大于空气,因此可选择E装置收集二氧化碳;
③若采取该装置采取向上排空气法收集二氧化碳,二氧化碳气体应从a管通入,使空气从上方的b管排出,实现向上排空气收集二氧化碳;
④实验室也可以使用固体二氧化锰与液体过氧化氢制取氧气,因此,无色气体也可能为氧气,反应的化学方程式为;由于氧气难溶于水且密度大于空气,因此可采取排水法或向上排空气法收集氧气,即选择装置C或E收集氧气;
故答案为:
(1)①该气体可能是CO2;把产生的气体通入澄清石灰水中,若石灰水变浑浊,则该气体为二氧化碳;(其他合理答案均可)
②B;E;
③a端进;
④2H2O2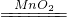 2H2O+O2↑;C或E;(其他合理答案均可)
2H2O+O2↑;C或E;(其他合理答案均可)
(2)50g 8%的氢氧化钠溶液中含氢氧化钠的质量=50g×8%=4g
设盐酸中氯化氢的质量为x,生成氯化钠质量为y
HCl+NaOH═NaCl+H2O
36.5 40 58.5
x 4g y
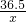 =
=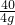 x=3.65g
x=3.65g
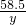 =
=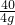 y=5.85g
y=5.85g
所用稀盐酸溶质的质量分数=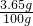 ×100%=3.65%
×100%=3.65%
反应后生成氯化钠溶液溶质的质量分数= ×100%=3.9%
×100%=3.9%
答:所用稀盐酸溶质的质量分数为3.65%;反应后生成氯化钠溶液溶质的质量分数为3.9%.
分析:(1)①根据药品的状态及反应条件,对照实验室制取气体的反应原理,猜想所制取的气体;并根据气体的性质,说明检验该气体的方法;
②根据所猜想气体的实验室制取所使用药品及反应条件,选择制取该气体的发生装置;根据气体的性质,选择收集气体的装置;
③根据该气体密度与空气密度的关系,判断使用该装置进行收集时的进气口;
④对气体进行再次猜想,并写出再次猜想气体的制取原理反应,及收集装置的选择;
(2)根据反应的化学方程式,由氢氧化钠的质量计算稀盐酸中溶质质量及反应生成氯化钠的质量,然后利用溶质质量分数公式,分别计算出所用稀盐酸及反应后所得溶液的溶质质量分数.
点评:利用固体物质与液体在常温下发生反应,可制取的气体有二氧化碳(石灰石与稀盐酸)、氢气(锌与稀硫酸)、氧气(二氧化锰与过氧化氢).
②由于制取二氧化碳使用块状固体与液体常温下反应制取,因此可选择B装置作为制取气体的发生装置;由于二氧化碳能溶于水且密度大于空气,因此可选择E装置收集二氧化碳;
③若采取该装置采取向上排空气法收集二氧化碳,二氧化碳气体应从a管通入,使空气从上方的b管排出,实现向上排空气收集二氧化碳;
④实验室也可以使用固体二氧化锰与液体过氧化氢制取氧气,因此,无色气体也可能为氧气,反应的化学方程式为;由于氧气难溶于水且密度大于空气,因此可采取排水法或向上排空气法收集氧气,即选择装置C或E收集氧气;
故答案为:
(1)①该气体可能是CO2;把产生的气体通入澄清石灰水中,若石灰水变浑浊,则该气体为二氧化碳;(其他合理答案均可)
②B;E;
③a端进;
④2H2O2
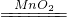 2H2O+O2↑;C或E;(其他合理答案均可)
2H2O+O2↑;C或E;(其他合理答案均可)(2)50g 8%的氢氧化钠溶液中含氢氧化钠的质量=50g×8%=4g
设盐酸中氯化氢的质量为x,生成氯化钠质量为y
HCl+NaOH═NaCl+H2O
36.5 40 58.5
x 4g y
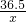 =
=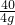 x=3.65g
x=3.65g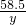 =
=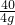 y=5.85g
y=5.85g所用稀盐酸溶质的质量分数=
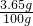 ×100%=3.65%
×100%=3.65%反应后生成氯化钠溶液溶质的质量分数=
 ×100%=3.9%
×100%=3.9%答:所用稀盐酸溶质的质量分数为3.65%;反应后生成氯化钠溶液溶质的质量分数为3.9%.
分析:(1)①根据药品的状态及反应条件,对照实验室制取气体的反应原理,猜想所制取的气体;并根据气体的性质,说明检验该气体的方法;
②根据所猜想气体的实验室制取所使用药品及反应条件,选择制取该气体的发生装置;根据气体的性质,选择收集气体的装置;
③根据该气体密度与空气密度的关系,判断使用该装置进行收集时的进气口;
④对气体进行再次猜想,并写出再次猜想气体的制取原理反应,及收集装置的选择;
(2)根据反应的化学方程式,由氢氧化钠的质量计算稀盐酸中溶质质量及反应生成氯化钠的质量,然后利用溶质质量分数公式,分别计算出所用稀盐酸及反应后所得溶液的溶质质量分数.
点评:利用固体物质与液体在常温下发生反应,可制取的气体有二氧化碳(石灰石与稀盐酸)、氢气(锌与稀硫酸)、氧气(二氧化锰与过氧化氢).

练习册系列答案
相关题目