题目内容
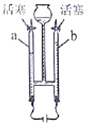
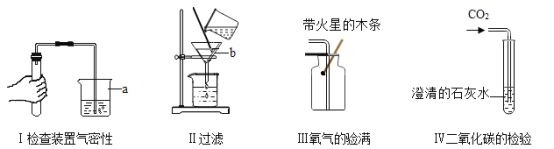
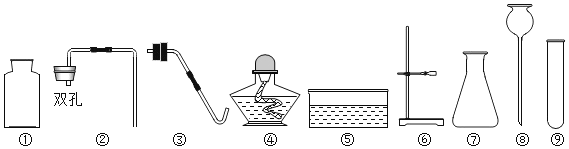
【题目】实验室用如图装置制取氧气。

(1)仪器a的名称是______。
(2)用高锰酸钾制取氧气的化学方程式是______。
(3)能用排水法收集氧气的原因是______。
(4)若收集到的氧气不纯,可能的原因是______(答1条即可)。
【答案】试管 2KMnO4![]() K2MnO4+MnO2+O2
K2MnO4+MnO2+O2![]() 氧气不易溶于水且不与水反应 导管口有气泡放出时,立即开始收集等
氧气不易溶于水且不与水反应 导管口有气泡放出时,立即开始收集等
【解析】
(1)由图可知,仪器a的名称是试管;
(2) 用高锰酸钾制取氧气的化学方程式是2KMnO4![]() K2MnO4+MnO2+O2
K2MnO4+MnO2+O2![]() ;
;
(3) 能用排水法收集氧气的原因是氧气不易溶于水且不与水反应;
(4) 收集到的氧气不纯,可能的原因是导管口有气泡放出时,立即开始收集,制取装置气密性不好,药品纯度不够等(答1条即可)

【题目】如表是 NaCl、NH4Cl 在不同温度时的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | |
(1)以上两种物质的溶解度受温度影响较大的是_____。
(2)40℃时,将 40.6g NaCl 加入到 100g 水中,充分搅拌使之溶解,所得溶液的质量为_____g。
(3)20℃时,NaCl 饱和溶液的溶质质量分数为(精确到小数点后 1 位)_____。
【题目】市场上的加碘食盐通常加入的是碘酸钾(KI03),替代了 原来的碘化钾(KI),因为碘化钾容易被氧气氧化为探究不同条件下KI与02的反应,进行如下系列实验。
(查阅资料)
①碘单质(I2)遇淀粉液变蓝。
②部分酸、碱、盐通常在水溶液中以离子形式存在。如:盐酸中存在H+和Cl-。
(进行实验)
实验1将不同浓度的KI溶液置于纯氧中,放置相同时间后观察,现象如下表:
装置 | 烧杯中的液体 | 现象 |
| ① 2mL0.15% KI 溶液 +5滴淀粉液 | 无明显变化 |
②2mL 1.5% KI 溶液 +5滴淀粉液 | 溶液变蓝 | |
③2mL 15% KI溶液+5 滴淀粉液 | 溶液变蓝,颜色较② 深 |
实验2将相同浓度的KI溶液加入不同浓度的稀盐酸后置于纯氧中,5分钟后观察,现象如下表:
烧杯中的液体 | 现象 | |
| ④ 2mL 15% KI溶液+5 滴淀粉液+2mL蒸 馏水 | 无明显变化 |
⑤2mL 15% KI溶液+5 滴淀粉液+2mL1%盐 酸 | 溶液变蓝 | |
⑥2mL15% KI溶液+5 滴淀粉液+2 mL 10% 盐酸 | 溶液变蓝,颜色较⑤ 深 |
(解释与结论)
(1)实验1的目的是______________。
(2)实验2中通过对比⑤和⑥,得出的结论是______________。
(3)实验2中,KI在盐酸的作用下与02反应的化学方程式如下,补全该反应的化学方程式:4KI+02+4HCI=4KCI+2_______+_______。
(反思与评价)
(4)实验④中加2mL蒸馏水的作用是______________。
(5)某同学将实验⑤中2mL10%盐酸替换成2mL10%NaCl溶液,5分钟后溶液颜色无明显变化,从离子角度分析,由此得出的结论是_____________________。