题目内容
水和溶液在生命活动和生活中起着十分重要的作用.
(1)海水中含有大量的氯化钠,可以通过________方法获得粗盐,粗盐提纯得到精盐.
(2)0.9%的氯化钠溶液称作生理盐水,其溶质是________.若用10%的NaCl溶液来配制100g 0.9%的氯化钠溶液,需加水________g.
(3)熟石灰在部分温度下的溶解度如下表所示.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 |
②采用一种操作方法,将上述烧杯中剩余固体全部溶解,变为不饱和溶液.下列说法正确的是________.
A.溶液的质量可能不变 B.溶液中溶质的质量分数一定减小
C.溶液中溶质的质量一定增大 D.可以升温使之变成不饱和溶液.
解:(1)氯化钠的溶解度受温度的影响不大,因此一般采用蒸发溶剂的方法得到氯化钠晶体;故答案为:蒸发溶剂
(2)生理盐水的溶质是氯化钠,用10%的NaCl溶液来配制100g0.9%的氯化钠溶液,由浓变稀,溶质不变,因此设加水的质量为x,(100g-x)×10%=100g×0.9%,x=91g;故答案为:氯化钠;91
(3)生石灰和水反应生成熟石灰,因此溶液中水的质量减少;因为形成的是20℃时的饱和溶液,所以按照100g水中最多溶解0.16g溶质计算质量分数即可;将上述烧杯中剩余固体全部溶解,变为不饱和溶液,说法正确的是:溶液中溶质的质量一定增大;溶液的质量一定变大,越升温越饱和.故答案为:①减小;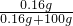 ×100%;②C
×100%;②C
分析:氯化钠的溶解度受温度的影响不大,因此一般采用蒸发溶剂的方法得到氯化钠晶体;生理盐水的溶质是氯化钠,用10%的NaCl溶液来配制100g 0.9%的氯化钠溶液,由浓变稀,溶质不变.生石灰和水反应生成熟石灰,因此溶液中水的质量减少;因为形成的是20℃时的饱和溶液,所以按照100g水中最多溶解0.16g溶质计算质量分数即可;将上述烧杯中剩余固体全部溶解,变为不饱和溶液,说法正确的是:溶液中溶质的质量一定增大;溶液的质量一定变大,越升温越饱和.
点评:本考点考查了结晶的原理、溶液中各成分的关系、溶质质量分数的公式和溶解度等,综合性比较强,要加强记忆,理解应用.本考点主要出现在填空题中.
(2)生理盐水的溶质是氯化钠,用10%的NaCl溶液来配制100g0.9%的氯化钠溶液,由浓变稀,溶质不变,因此设加水的质量为x,(100g-x)×10%=100g×0.9%,x=91g;故答案为:氯化钠;91
(3)生石灰和水反应生成熟石灰,因此溶液中水的质量减少;因为形成的是20℃时的饱和溶液,所以按照100g水中最多溶解0.16g溶质计算质量分数即可;将上述烧杯中剩余固体全部溶解,变为不饱和溶液,说法正确的是:溶液中溶质的质量一定增大;溶液的质量一定变大,越升温越饱和.故答案为:①减小;
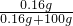 ×100%;②C
×100%;②C分析:氯化钠的溶解度受温度的影响不大,因此一般采用蒸发溶剂的方法得到氯化钠晶体;生理盐水的溶质是氯化钠,用10%的NaCl溶液来配制100g 0.9%的氯化钠溶液,由浓变稀,溶质不变.生石灰和水反应生成熟石灰,因此溶液中水的质量减少;因为形成的是20℃时的饱和溶液,所以按照100g水中最多溶解0.16g溶质计算质量分数即可;将上述烧杯中剩余固体全部溶解,变为不饱和溶液,说法正确的是:溶液中溶质的质量一定增大;溶液的质量一定变大,越升温越饱和.
点评:本考点考查了结晶的原理、溶液中各成分的关系、溶质质量分数的公式和溶解度等,综合性比较强,要加强记忆,理解应用.本考点主要出现在填空题中.

练习册系列答案
相关题目
(6分)水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)净水器中经常使用活性炭,主要利用活性炭的_______性。
(2)根据图中实验只生成了氢气和氧气,确定水是由氢元素和氧元素组成的,得到此结论的依据是________。写出此实验中发生反应的化学方程式________。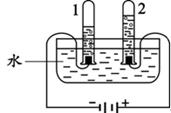
(3)烧杯中盛有一定质量、温度为80℃、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量。测定结果记录如下表。
| 溶液的温度/℃ | 75 | 65 | 50 | 35 | 20 |
| 析出固体M的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |
① 65℃时,该溶液是否为饱和溶液? (填“是”、“否”或“无法判断”);
②将t℃时接近饱和的M溶液变成饱和溶液,下列方法中一定能达到目的的是 (填字母序号);
A. 升温 B. 降温 C. 加溶质M
D. 加水 E. 加另一种固体N F. 恒温蒸发水
G. 与t℃时M的饱和溶液混合
③ 20℃时,用固体粉末M和水配制100g溶质质量分数为5%的M溶液,必须用到的仪器有:托盘天平(带砝码)、烧杯、 。
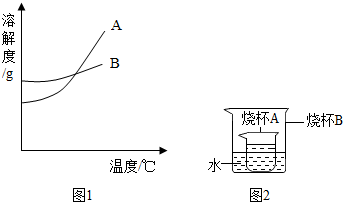 (2013?通州区一模)水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与溶解度曲线(图1),回答下列问题:
(2013?通州区一模)水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与溶解度曲线(图1),回答下列问题: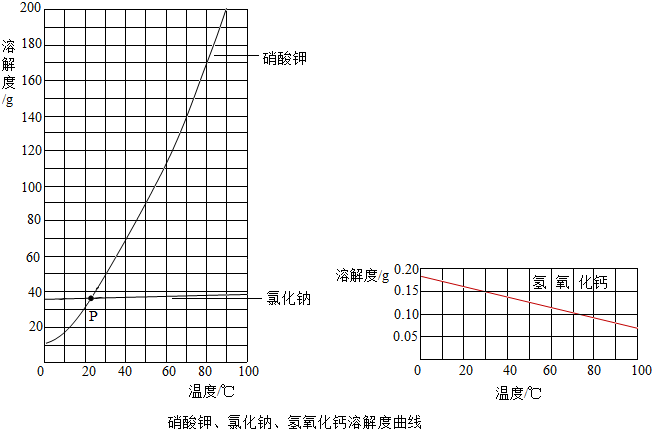
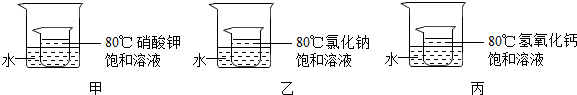
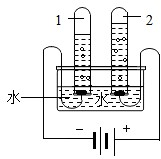 (2012?昌平区二模)水和溶液在生命活动和生产、生活中起着十分重要的作用.
(2012?昌平区二模)水和溶液在生命活动和生产、生活中起着十分重要的作用.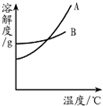 水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与
水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与