题目内容
【题目】在化学实验室里和日常生活中我们常常将固体药品配制成溶液进行化学反应。
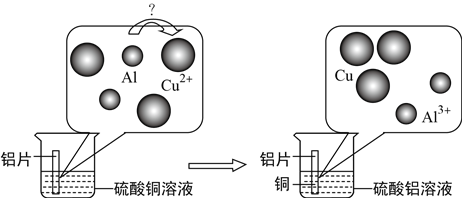
(1)下图所示为氯化钠加入水中发生变化的微观过程示意图。
Ⅰ图表示氯化钠固体加入水中。
Ⅱ图表示水分子作用在氯化钠固体上。
Ⅲ图表示氯化钠固体以__________和__________(填写粒子符号)的形式向水中扩散,最终均一地分散到水分子中。

(2)如图是某试剂瓶标签上的内容。
浓硫酸(分析纯)
化学式:H2SO4 相对分子质量:98
密度:1.84g/cm3 质量分数:98%
①把这种浓硫酸稀释为19.6%的硫酸溶液200g需要这种浓硫酸的体积为__________mL(保留一位小数),需要水__________mL。
②稀释浓硫酸时,应注意的事项为__________。
A.直接在量筒中稀释 B.转移在烧杯中稀释
C.把浓硫酸沿器壁慢慢注入水中 D.把水沿器壁慢慢注入浓硫酸中
E.用玻璃棒不断搅拌
【答案】 Na+ Cl- 21.7 160 BCE
【解析】(1)NaCl固体加入水中之后会电离出Na+、Cl-,故以Na+、Cl-的形式存在;
(2)①浓硫酸质量为![]()
则体积为![]() ,所注水质量200g-40g=160g,即为160mL。
,所注水质量200g-40g=160g,即为160mL。
②稀释浓H2SO4时应在烧杯中进行,不能在量筒中进行;稀释浓H2SO4应将浓H2SO4注入水中,应用玻璃棒缓慢搅拌,故选BCE。

练习册系列答案
相关题目