题目内容
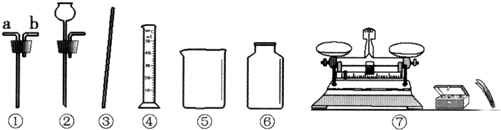
如图所示,现有以下实验仪器,请按要求填空:
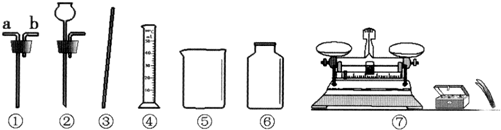
(1)图中仪器⑤的名称
(2)配制一定质量分数的氯化钠溶液,需用到的仪器有
(3)某同学利用仪器①与⑥组合成一个贮气装置.当装满水用排水法收集甲烷(甲烷难溶于水、其密度比空气小)时,气体应从仪器①的
(4)下列对某些实验现象或实验操作的叙述正确的是
①铁丝在空气中燃烧产生淡蓝色火焰;
②镁条在空气中燃烧发出耀眼的白光;
③将CO还原Fe2O3的尾气直接排入空气;
④不慎将氢氧化钠溶液沾在皮肤上,要用较多的水冲洗,再涂上稀硼酸溶液.

(1)图中仪器⑤的名称
烧杯
烧杯
(2)配制一定质量分数的氯化钠溶液,需用到的仪器有
③④⑤⑦
③④⑤⑦
(填序号),如果实验室用上述仪器中的②与⑥组合成制取CO2气体装置,此反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)某同学利用仪器①与⑥组合成一个贮气装置.当装满水用排水法收集甲烷(甲烷难溶于水、其密度比空气小)时,气体应从仪器①的
b
b
(填“a”或“b”)通人;集满甲烷后将其导出使用时,水应该从仪器①的a
a
(填“a”或“b”)导入.(4)下列对某些实验现象或实验操作的叙述正确的是
②④
②④
①铁丝在空气中燃烧产生淡蓝色火焰;
②镁条在空气中燃烧发出耀眼的白光;
③将CO还原Fe2O3的尾气直接排入空气;
④不慎将氢氧化钠溶液沾在皮肤上,要用较多的水冲洗,再涂上稀硼酸溶液.
分析:(1)熟悉常用仪器;
(2)考虑配制一定质量分数的氯化钠溶液的步骤是:计算、称量、溶解.然后再想各个步骤中要用到的仪器;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳;
(3)根据装置的特点结合甲烷的性质进行分析;
(4)根据所学知识逐一分析即可.如铁丝不能在空气中燃烧,而镁条可以,并发出白光;一氧化碳有毒不能直接排放到空气中等,即可确定答案.
(2)考虑配制一定质量分数的氯化钠溶液的步骤是:计算、称量、溶解.然后再想各个步骤中要用到的仪器;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳;
(3)根据装置的特点结合甲烷的性质进行分析;
(4)根据所学知识逐一分析即可.如铁丝不能在空气中燃烧,而镁条可以,并发出白光;一氧化碳有毒不能直接排放到空气中等,即可确定答案.
解答:解:(1)熟悉常用仪器,了解它们的名称,图中⑤是烧杯,故答案为:烧杯;
(2)配制一定质量分数的氯化钠溶液的步骤是:计算、称量、溶解,据此可知,要用到得仪器有:托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒,观察图形可知,图中需用到的仪器有:③④⑤⑦;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.故答案为:③④⑤⑦;CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)当装满水用排水法收集甲烷时,甲烷的密度比水小,因此气体应从仪器①的b端通人;集满甲烷后将其导出使用时,水应该从仪器①的a端导入,甲烷冲b导出.
故答案为:b;a;
(4)铁丝不能在空气中燃烧,故①不正确;
镁条能在空气中燃烧发出耀眼的白光,故②正确;
一氧化碳有剧毒,当用它还原氧化铁时,可能会有没发生反应的一氧化碳,所以尾气不能直接排到空气中,故③不正确;
氢氧化钠溶液是强碱具有腐蚀性,如果不慎将氢氧化钠溶液沾在皮肤上,要用较多的水冲洗,再涂上稀硼酸溶液,故④正确;
故选②④.
(2)配制一定质量分数的氯化钠溶液的步骤是:计算、称量、溶解,据此可知,要用到得仪器有:托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒,观察图形可知,图中需用到的仪器有:③④⑤⑦;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.故答案为:③④⑤⑦;CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)当装满水用排水法收集甲烷时,甲烷的密度比水小,因此气体应从仪器①的b端通人;集满甲烷后将其导出使用时,水应该从仪器①的a端导入,甲烷冲b导出.
故答案为:b;a;
(4)铁丝不能在空气中燃烧,故①不正确;
镁条能在空气中燃烧发出耀眼的白光,故②正确;
一氧化碳有剧毒,当用它还原氧化铁时,可能会有没发生反应的一氧化碳,所以尾气不能直接排到空气中,故③不正确;
氢氧化钠溶液是强碱具有腐蚀性,如果不慎将氢氧化钠溶液沾在皮肤上,要用较多的水冲洗,再涂上稀硼酸溶液,故④正确;
故选②④.
点评:本题考查实验仪器的选取和常见的实验现象,需要同学们对常见实验仪器和现象做到心中有数.

练习册系列答案
相关题目
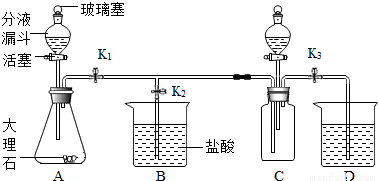
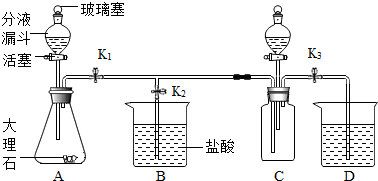 (2012?丰台区一模)化学兴趣小组用如图所示装置进行以下实验.
(2012?丰台区一模)化学兴趣小组用如图所示装置进行以下实验.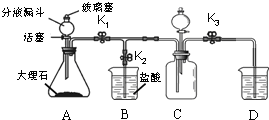 化学兴趣小组用如图所示装置进行以下实验.
化学兴趣小组用如图所示装置进行以下实验.