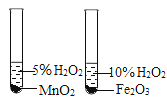题目内容
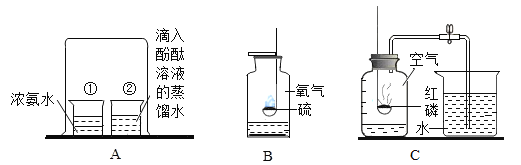
【题目】请你一起参与完成以下两个实验.
[实验一]探究“锡纸”中金属的成分:“锡纸”中的金属是锡吗?
[查阅资料]
①“锡纸”是锡箔或铝箔和纸黏合而成;
②锌粉是一种深灰色固体;
③锡(Sn)与酸或金属化合物溶液反应生成+2价的锡的化合物。
[提出猜想]
猜想I:“锡纸”中的金属是锡;
猜想II:“锡纸”中的金属是铝。
[进行实验]设计方案并进行实验
实验操作 | 实验现象 | 实验分析与结论 |
取打磨后的“锡纸”片放入试管中,滴加氯化锌溶液 | “锡纸”表面有深灰色固体析出 | 根据实验现象,结合金属活动性顺序可知猜想_______(选填“Ⅰ”或“Ⅱ”)成立;反应的化学方程式为________; |
[交流讨论]
① 实验中打磨“锡纸”的目的是__________;
②下列物质的溶液可以替代氯化锌溶液完成上述实验的是_________.(填序号)
A 氯化铜
B 硫酸亚铁
C 硫酸钠
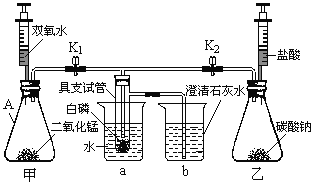
[实验二]甲、乙两位同学利用图中的装置,围绕“用称量的方法验证化学反应是否遵守质量守恒定律并分析实验条件”这一探究目的开展活动.
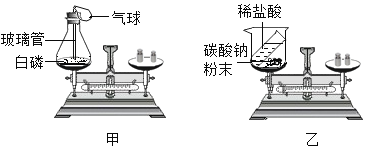
[实验分析]
(1)请你仿照示例,完成实验现象的记录和分析
实验现象 | 是否遵循质量守恒定律 | |
甲同学 | 白磷_________;气球_______;托盘天平_________; | 该反应遵守质量守恒定律 |
乙同学 | 烧杯内有气泡产生,反应前后托盘天平不平衡 | 该反应不遵守质量守恒定律 |
通过对上述实验的对比分析,你认为_______; (填“甲”或“乙”)的结论是错误的.在实验操作完全正确的情况下,请分析实验结论错误的原因________;
[实验结论]化学反应都遵守质量守恒定律。
[实验反思](2)请从微观角度分析化学反应遵守质量守恒定律的原因是________。
【答案】II 2Al+3ZnCl2=3Zn+2AlCl3 除去表面氧化物 B 燃烧,产生大量白烟,放出大量热 先变大后变小 先向右偏后平衡 乙 反应生成二氧化碳气体逸散到空气中导致反应前后托盘天平不平衡 化学反应前后,原子的种类、数目、质量都不变
【解析】
实验操作 | 实验现象 | 实验分析与结论 |
取打磨后的“锡纸”片放入试管中,滴加氯化锌溶液 | “锡纸”表面有深灰色固体析出 | 根据实验现象,结合金属活动性顺序可知猜想Ⅱ成立;因为铝的活泼性比锌强,反应的化学方程式为2Al+3ZnCl2=3Zn+2AlCl3; |
① 实验中打磨“锡纸”的目的是:除去表面氧化物,防止影响实验;
②下列物质的溶液可以替代氯化锌溶液完成上述实验的是
A 氯化铜,铜的活泼性比锡弱,不能代替;
B 硫酸亚铁,铁的活泼性比锡强,比铝弱,可以代替;
C 硫酸钠,钠的活泼性比铝强,不能代替;
故选:B。
(1)请你仿照示例,完成实验现象的记录和分析
实验现象 | 是否遵循质量守恒定律 | |
甲同学 | 白磷燃烧,产生大量白烟,放出大量热;气球气球先变大后变小;托盘天平托盘天平先向右偏后平衡; | 该反应遵守质量守恒定律 |
乙同学 | 烧杯内有气泡产生,反应前后托盘天平不平衡 | 该反应不遵守质量守恒定律 |
通过对上述实验的对比分析,你认为乙的结论是错误的.在实验操作完全正确的情况下,请分析实验结论错误的原因:反应生成二氧化碳气体逸散到空气中导致反应前后托盘天平不平衡;
[实验结论]化学反应都遵守质量守恒定律。
[实验反思](2)请从微观角度分析化学反应遵守质量守恒定律的原因是:化学反应前后,原子的种类、数目、质量都不变。

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案【题目】实验设计能实现其对应的实验目的是
|
|
|
|
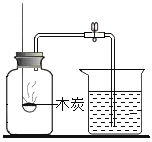
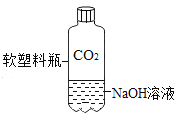
A. 测定空气中O2 的含量 | B. 证明 CO2 与NaOH溶液反应 | C. 比较 MnO2 和Fe2O3 的催化效果 | D. 此装置具有“启普发生器”的功能 |
A.AB.BC.CD.D
【题目】乙醇不完全燃烧时产生CO、CO2和H2O。依据下表数据分析得出的结论中,不正确的是:
物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | 一氧化碳 |
反应前质量/g | 6.6 | 8.8 | 0 | 0 | 0 |
反应后质量/g | 2 | 0 | 6.6 | 5.4 | a |
A. 表中的a值为1.4 B. 在化学反应前后碳元素质量一定相等
C. 参加反应的乙醇和氧气的质量比为3:4 D. 生成的CO和CO2分子个数比为1:3