题目内容
【题目】(10分)某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红。碱溶液可以使酚酞试液变红,是因为碱在水中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞试液变红呢?他们设计了如图三个实验,请你和他们一起探究并完成下列问题:
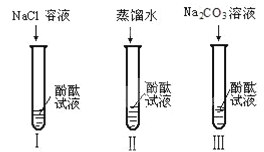
(1)实验Ⅰ是为了
(2)实验Ⅱ加入蒸馏水的目的是探究水分子是否能使酚酞试液变红,小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是 ;
(3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞试液变红,向变红后的溶液中再逐滴滴入过量的CaCl2溶液,红色逐渐消失,同时还观察到生成 ,反应的化学方程式______________________________。由实验Ⅰ、Ⅱ、Ⅲ得出结论:CO32-可以使酚酞试液变红;
(4)小组同学在与老师交流上述结论时,老师说:“其实Na2CO3溶液能使酚酞试液变红也是由于溶液中存在OH-”。你认为Na2CO3溶液中存在OH-的原因是________________________。
【答案】(1)探究钠离子是否能使酚酞试液变红
(2)氯化钠溶液中含有水分子
(3)生成白色沉淀 Na2CO3+ CaCl2==2NaCl+CaCO3↓
(4)碳酸根离子与水反应生成氢氧根离子
【解析】
试题分析:碳酸钠溶液中含有钠离子、碳酸根离子和水分子。
(1)加入氯化钠相当于加入了钠离子,目的是探究钠离子是否能使酚酞试液变红;
(2)由于加入的氯化钠溶液中含有水分子,故不需要再加入水来验证;
(3)碳酸钠会与氯化钙反应生成碳酸钙沉淀和氯化钠:Na2CO3+ CaCl2==2NaCl+CaCO3↓,看到的现象是产生白色沉淀;
(4)碳酸钠中的碳酸根离子与水反应会生成氢氧根离子,导致溶液呈碱性。

 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案