题目内容
【题目】生活中处处有化学,请你根据所学的化学知识用化学式填空。
(1)抢救危重病人常用的气体单质是 ;
(2)地壳中含量最多的元素和含量最多的金属元素形成的化合物是___________;
(3)既可作为消毒剂,也可用于实验室制取氧气的液体试剂是 ;
(4)易与血红蛋白结合使人中毒的氧化物是 。
【答案】(1)O2(2)Al 2O3(3) H2O2(4) CO
【解析】试题分析:(1)氧气可供给呼吸,因此可抢救危重病人;(2)地壳中最多的元素为O显-2价,最多的金属元素为Al显+3价,因此组成的化合物为Al 2O3;(3)应为过氧化氢H2O2(4)为CO。

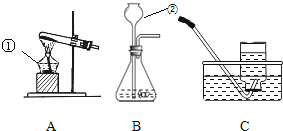
【题目】如图所示,某校化学兴趣小组用过氧化氢(H2O2)溶液(MnO2作催化剂)制取干燥的氧气,并用来侧定,10g某铜粉样品(含杂质碳)中铜的质量分数.回答下列问题:

(1)仪器a的名称是 .
(2)装置A中发生反应的化学方程式是 .装置B的作用是 .
(3)通过称量反应前后装置 的质量,进行计算便可求出样品中铜的质量分数.
(4)实验完毕.小丽同学误将用剩的H202溶液和装置C玻璃管中的剩余固体一起倒入烧杯中,发现有大最的气泡产生,经检验确认产生的气体是氧气.小刚和小明两位同学对此颇感兴趣.进而展开了他们的探究之旅.
【提出问题】是哪种物质加快了H202的分解速率?
【大胆猜想】猜想Ⅰ:剩余固体中的氧化铜加快了H202溶液的分解.
猜想Ⅱ:剩余固体中的 加快了H2O2溶液的分解.
猜想Ⅲ:氧化铜能做H202分解的催化剂.
【实验验证】
实验方案 | 实验现象 | 分析及结论 |
实验一:将带火星的木条伸入盛有5mL 5%H2O2溶液的试管. | 带火星木条不复燃 | H202溶液常温下产生氧气的量很少,不足以使带火星的木条复燃 |
实验二:向盛有5mL5%H202溶液的试管中加入1g氧化铜固体,将一根带火星的木条伸入试管.观察现象.待反应结束后将试管里的剩余物进行 、洗涤、干燥、称量.对比反应前后氧化铜的质量 | 称得固体质量为1g. | 猜想Ⅰ成立.反应前后氧化铜的质量相等. |
实验三:向盛有5mL5%H202溶液的试管中加入1g ,将一根带火星的木条伸入试管,观察现象. | 没有气泡产生,带火星 木条不复燃. | 猜想Ⅱ (填”成立“或“不成立”) |
【讨论交流】小刚同学认为,根据实验二得出的两个结论就能判断Ⅲ成立,你是否支持他的观点?并简述理由。
答: 。 .