题目内容
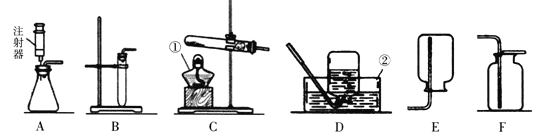
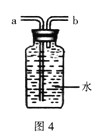
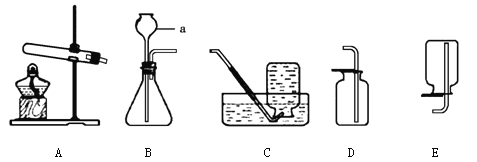
【题目】(7分)科学探究是奇妙的过程,再一次实验中小文不小心把硫酸铁溶液滴加到了盛有5%H 2 O 2 的溶液的试管中,立即有大量的气泡产生.硫酸铁溶液中含有三种粒子(H2O、SO42-、Fe3+),小文想知道硫酸铁溶液中的哪种粒子能使双氧水分解的速率加快.请你和小文一起通过下图所示的三个实验完成这次探究活动,并填写空白.

(1)你认为最不可能的是哪一种粒子________,理由是 .
(2)检验实验产生的气体是否是氧气的方法是 .
(3)在实验②中加入稀硫酸后,无明显变化,说明________不起催化作用;
(4)小明如果要确定硫酸铁是催化剂,还须通过实验确认它在化学反应前后______________.
(5)经证明硫酸铁是过氧化氢分解的催化剂,写出硫酸铁催化过氧化氢分解的化学方程式____________.
注意:若答对(6)小题奖励4分,但化学试卷总分不超过60分。
(6)小华通过实验发现,硫酸铁溶液的浓度也会影响过氧化氢分解的速率,常温下,他在a,b,c,三个试管中分别加入等量5%过氧化氢的溶液,在其他条件相同时,各滴2滴5%、10%、20%的硫酸铁溶液。根据实验数据绘制了产生的氧气体积和时间变化的曲线如图。请你观察右图回答问题。
①写出两条规律性结论:____________。
②若实验中所得的曲线如图中虚线所示,请推测其中可能的原因____________。

【答案】(1)水分子;过氧化氢溶液中已经含有水分子;
(2)把带火星的木条伸入试管中,若木条复燃则是氧气;(3)SO42-;
(4)质量和化学性质不变;
(5)![]() ;
;
(6)硫酸铁溶液浓度越大,过氧化氢分解的反应速率越大;硫酸铁溶液的浓度不会影响最终产生的氧气质量;其它条件相同是,过氧化氢的浓度变大(合理即可)。
【解析】
试题分析:(1)含有的微粒有过氧化氢分子,水分子,铁离子,硫酸根离子,过氧化氢溶液中已经含有水分子因此最不可能的就是水分子;(2)氧气浓度越高燃烧越剧烈;(3)硫酸中有水分子、氢离子、硫酸根离子,这里有关系的就是硫酸根离子;(4)催化剂是能改变反应速率但质量和化学性质不变,已经证明能改变反应速率了,那么就还需证明质量和化学性质不变;(5)略;(6)该实验的变量为硫酸铁溶液的浓度,a﹤b﹤c,同时反应速率也是a﹤b﹤c,可以得出硫酸铁溶液浓度越大,过氧化氢分解的反应速率越大;又虽然反应速率不同但气体量都一样因此硫酸铁溶液的浓度不会影响最终产生的氧气质量;虚线反应速率更大,气体量更多,因此是过氧化氢的浓度变大。

 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案【题目】在一个密闭容器中加入四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 3 | 5 | 20 | 7 |
反应后质量/g | 10 | 5 | 8 | 待测 |
通过分析,判断下列说法正确的是
A.测得反应后丁物质的质量为12g B.乙物质一定是催化剂
C.该反应是化合反应 D.该反应中甲、丙的质量比为5:4