题目内容
某中学的九年级(1)班同学去太行山春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
试回答:
(1)10.0g样品与45.0g盐酸充分反应后,盐酸是否还剩余 (填“是”或“否”),样品中碳酸钙的质量分数是 .
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?所用稀盐酸的溶质质量分数为多少?(计算结果精确到小数点后两位).
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入盐酸的质量(g) | 20.0 | 30.0 | 45.0 | 50.0 |
| 剩余固体的质量(g) | 6.0 | 4.0 | 1.0 | 1.0 |
(1)10.0g样品与45.0g盐酸充分反应后,盐酸是否还剩余
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?所用稀盐酸的溶质质量分数为多少?(计算结果精确到小数点后两位).
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)①由甲同学可知完全反应的20.0克盐酸消耗了(10-6)克样品中的固体“推导出(10-1)克样品中的固体与45.0克盐酸恰好完全反应,从而判断盐酸没有剩余.
②由图表可知,完全反应后剩余固体是杂质,质量为1.0g,据此计算出石灰石样品中碳酸钙的质量,然后根据质量分数公式就可计算出样品中碳酸钙的质量分数;
(2)根据碳酸钙与盐酸反应的化学方程式和CaCO3的质量,列出比例式,就可计算出生成二氧化碳的质量,所用稀盐酸的溶质质量分数.
②由图表可知,完全反应后剩余固体是杂质,质量为1.0g,据此计算出石灰石样品中碳酸钙的质量,然后根据质量分数公式就可计算出样品中碳酸钙的质量分数;
(2)根据碳酸钙与盐酸反应的化学方程式和CaCO3的质量,列出比例式,就可计算出生成二氧化碳的质量,所用稀盐酸的溶质质量分数.
解答:解:
(1)①由甲同学可知完全反应的20.0克盐酸消耗了(10-6)克样品中的固体“推导出(10-1)克样品中的固体与45.0克盐酸恰好完全反应,从而判断盐酸没有剩余.
②样品中碳酸钙的质量分数为
×100%=90%;
(2)设生成二氧化碳的质量为x,所用稀盐酸的溶质质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
10g×90% y x
=
x=3.96g.
=
y=6.57g
所用稀盐酸的溶质质量分数
×100%=14.6%
答案:
(1)否 90%
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳3.96克,所用稀盐酸的溶质质量分数为14.6%
(1)①由甲同学可知完全反应的20.0克盐酸消耗了(10-6)克样品中的固体“推导出(10-1)克样品中的固体与45.0克盐酸恰好完全反应,从而判断盐酸没有剩余.
②样品中碳酸钙的质量分数为
| 10g-1g |
| 9g |
(2)设生成二氧化碳的质量为x,所用稀盐酸的溶质质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
10g×90% y x
| 100 |
| 44 |
| 10g×90% |
| x |
x=3.96g.
| 100 |
| 73 |
| 10g×90% |
| y |
y=6.57g
所用稀盐酸的溶质质量分数
| 6.57g |
| 45g |
答案:
(1)否 90%
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳3.96克,所用稀盐酸的溶质质量分数为14.6%
点评:本题主要考查学生对完全反应的认识,以及利用化学方程式进行计算的能力.考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
对如图四幅图的相关说法中不正确的是( )
A、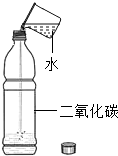 向装有二氧化碳的塑料瓶中倒水,拧紧瓶盖、振荡、塑料瓶变瘪. 如图:因为二氧化碳能溶于水且能与水反应,所以塑料瓶变瘪 |
B、 向装有二氧化锰的锥形瓶中加过氧化氢溶液,反应速率加快. 如图:因为MnO2对H2O2具有催化作用,所以反应速率加快 |
C、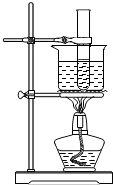 用酒精灯给烧杯中的水加热 如图:因为液体沸腾时需要吸热,所以试管中的水一会儿就会沸腾 |
D、 ②中尖嘴导管口有“喷泉”产生 如图:烧瓶中所加物质为铝粉和稀盐酸 |

 一年的化学学习,我们亲身体验了一系列的探究实验,感受到了化学的无穷魅力.下面就让我们一起回顾硫酸型酸雨形成的模拟实验:
一年的化学学习,我们亲身体验了一系列的探究实验,感受到了化学的无穷魅力.下面就让我们一起回顾硫酸型酸雨形成的模拟实验: