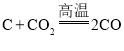题目内容
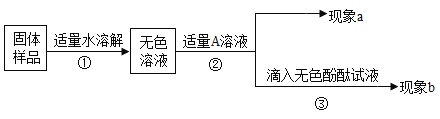
【题目】下列关系图中,“—”表示两端的物质能发生化学反应,“→”表示物质的转化方向。
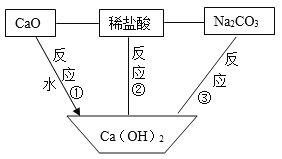
(1)反应①的化学方程式为_____________________________,该反应_____热量(填“放出”或“吸收”)。
(2)反应②的化学方程式为_________,若稀盐酸与 氢氧化钙恰好完全反应,所得溶液呈_____(填“酸性”、“碱性”或“中性”)。
(3)反应③可制得 NaOH,其化学方程式为_____________。
【答案】CaO + H2O = Ca(OH)2 放出 2HCl+ Ca(OH)2 = CaCl 2 + 2 H2O 中性 Na2CO3 + Ca(OH)2 = CaCO3↓ +2NaOH
【解析】
氧化钙和水生成氢氧化钙,稀盐酸和氢氧化钙生成氯化钙和水,碳酸钠和氢氧化钙生成氢氧化钠和碳酸钙。
(1)反应①是氧化钙和水生成氢氧化钙,反应的化学方程式为CaO+H2O=Ca(OH)2,该反应放出热量。
(2)反应②是稀盐酸和氢氧化钙生成氯化钙和水,反应的化学方程式为2HCl+ Ca(OH)2=CaCl2+2H2O,若稀盐酸与氢氧化钙恰好完全反应,生成物是氯化钙和水,故所得溶液呈中性。
(3)反应③可制得NaOH,碳酸钠和氢氧化钙生成氢氧化钠和碳酸钙,反应的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。

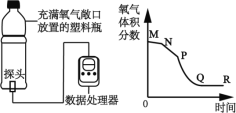
【题目】当空气中的CO2含量超过一定量时会影响人体健康。
[查阅资料]空气中CO2的体积分数为1%时,人会有心跳加快、困乏、注意力不集中、轻度恶心等症状;体积分数为5%时,会有呼吸不畅、头晕、耳鸣、血压升高等症状;体积分数为10%时,会有严重缺氧、丧失意识、昏迷等症状。
[提出问题]在没有专业测量仪器的情况下,如何检验空气中CO2的含量已经达到影响人体健康的程度?
[设计实验]依据CO2的性质,设计检验方法。
CO2性质 | 检验方法 | 预期现象 | |
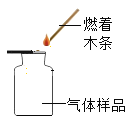
方法1 | (1) | 用燃着木条检验 | 燃着木条熄灭 |
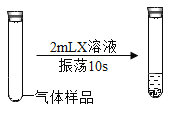
方法2 | 与水反应 | 用X溶液检验 | 溶液由紫色变为红色 |
方法3 | 与石灰水反应 | 用澄清石灰水检验 | 溶液中产生白色浑浊 |
(1)方法1依据的CO2性质是_______________。
(2)根据方法2的预期现象推断,所需试剂X是___________溶液。
(3)用化学方程式表示方法3的原理:_____________。
[配制样品]常温常压下,配制CO2体积分数不同的气体样品。
(4)收集5mLCO2与空气混合,得到500 mL 1%的气体样品;收集25 mL CO2与空气混合,得到500 mL_______%的气体样品。
[进行实验]常温常压下,集气瓶和试管中盛有空气或CO2气体样品,分别进行以下实验。
方法1 | 方法2 | 方法3 | |
实验过程 |
|
|
|
空气 | 正常燃烧 | 溶液无明显变化 | 溶液无明显变化 |
1%的CO2气体样品 | 正常燃烧 | 溶液无明显变化 | 溶液中产生白色浑浊 |
5%的CO2气体样品 | 正常燃烧 | 溶液由紫色变为红色 | 溶液中产生白色浑浊 |
[解释与应用]
(5)从灭火原理分析,方法1中均没有出现“燃着木条熄灭”的原因是________________。
(6)1班有部分同学在教室内出现“困乏、注意力不集中”等症状时,小林同学想用上述实验方法检测教室内CO2气体的含量,他应该选用的方法是__________(填方法序号)。
(7)2班小瑜同学收集了教室中的气体,尝试用方法2进行实验,发现溶液由紫色变为红色。由此现象推测此时教室中CO2的含量可能为___________(填字母序号)。
A1%以下 B1% C1%~ 5% D5%以上