题目内容
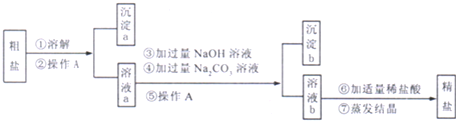
【题目】高纯碳酸锰(MnCO3)有广泛的用途,采用工业硫酸锰制备流程如下:
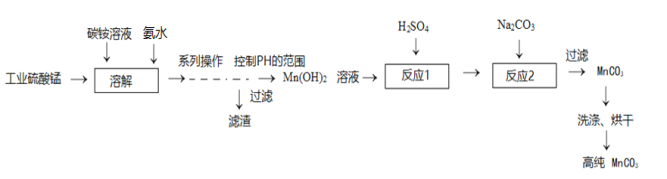
已知:MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀的pH=7.7。
(1)系列操作后“控制pH的范围_____(填>、<、=)7.7。
(2)反应1属于基本反应类型中的_____(填“置换反应”“中和反应”“复分解反应”)。
(3)写出反应2的化学方程式_____,洗涤剂最好选择乙醇的原因_____,烘干在_____(填>、<、等于=)100°C的真空中进行。
【答案】< 复分解反应 MnSO4+Na2CO3=Na2SO4+MnCO3↓ 洗去表面的杂质,便于快速干燥,且能防止氧化而变质 <
【解析】
(1)Mn(OH)2开始沉淀的pH=7.7,所以系列操作后控制pH<7.7,防止生成Mn(OH)2沉淀。
(2)反应1为氢氧化锰和稀硫酸反应生成硫酸锰和水,该反应属于复分解反应,也属于中和反应,但中和反应不是基本反应类型。
(3)反应2为硫酸锰和碳酸钠反应生成碳酸锰沉淀和硫酸钠,反应的方程式为:MnSO4+Na2CO3=Na2SO4+MnCO3↓。洗涤剂选用乙醇的原因为:MnCO3难溶于乙醇,乙醇可以洗去表面的杂质,易挥发便于快速干燥,且能防止氧化。MnCO3潮湿时易被空气氧化,100℃开始分解,故烘干在<100°C的真空中进行。

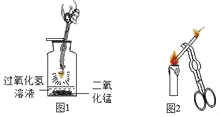
【题目】合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.
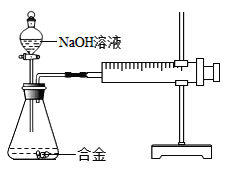
(提出问题)难道NaOH溶液也能与某些金属发生化学反应吗?
(查阅资料)(1)铝能与氢氧化钠溶液反应,铁、铜不能与氢氧化钠溶液反应.
(2)铝与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑(NaAlO2溶于水,溶液显无色)
(进行猜想)猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有_____.
猜想3:该合金粉末中除铝外,还含有铁、铜.
(实验探究)下列实验(见表1)仅供选用的试剂:20%的硫酸溶液、30%的NaOH溶液.
表1实验记录
实验步骤 | 实验现象 | 结论 |
①取一定量的合金粉末,加过量的_____,充分反应后过滤,滤渣备用 | 粉末部分溶解,并有无色气体放出 | 合金中一定含有_____. |
②取步骤①所得滤渣,加过量_____,充分反应 | 滤渣部分溶解,并有无色气体放出,溶液呈浅绿色 | 合金中一定含有 _____ |
(得出结论)猜想3成立.
(反思)
一般来说,活泼金属能与稀硫酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.若小明向合金粉末中加入的是足量的稀硫酸,则最终剩余的固体成分是_____.
(拓展与分析)请你设计一个实验方案,比较铝、铁、铜的金属活动性强弱_____.