题目内容
金属与酸反应速率与酸液的浓度有关,在一定量的硫酸溶液加入一定质量的金属铝,反应速率较快,为了使反应速率减慢,又不影响产生氢气的质量,下列措施不可行的是
- A.加入适量的氯化钡溶液
- B.加入适量的硫酸铜溶液
- C.加入适量的硫酸钠溶液
- D.加入适量的蒸馏水
B
分析:酸液的浓度越小,反应速度越快.为使一定质量的金属铝与一定量的硫酸溶液的反应速率减慢,可减小酸液的浓度,当加入ABCD四选项中的物质时,均能减小酸液的浓度,起到减缓反应速率的作用,但是当加入硫酸铜溶液时,由于金属铝比铜活泼,金属铝先与硫酸铜溶液发生如下反应:Fe+CuSO4═Cu+FeSO4,这样减少了与酸反应的金属铝的质量,从而影响到产生氢气的质量,与题目要求又不影响产生氢气的质量不符.故答案B不可行.
解答:A、加入适量的氯化钡溶液,尽管发生如下反应:BaCl2+H2SO4═BaSO4↓+2HCl 只是H+的浓度减小但质量不变,故反应速率减慢,又不影响氢气的质量,该措施可行.
B、加入适量的硫酸铜溶液,金属铝先与硫酸铜溶液发生如下反应:Fe+CuSO4═Cu+FeSO4,这样减少了与酸反应的金属铝的质量,从而影响到产生氢气的质量,故该措施不可行.
C、硫酸钠与硫酸和金属铝都不反应,加入适量的硫酸钠溶液后,只是增加了溶液的质量,降低了酸液的浓度,故能使反应速率减慢,又不影响氢气的质量,该措施可行.
D、加入适量的蒸馏水,稀释了酸液,故能使反应速率减慢,又不影响氢气的质量,该措施可行.
故选:B
点评:该题难度不大,但综合性较强,以影响反应速率的因素探究为情境,重点考查金属活动顺序的应用和对溶质质量分数的理解.
分析:酸液的浓度越小,反应速度越快.为使一定质量的金属铝与一定量的硫酸溶液的反应速率减慢,可减小酸液的浓度,当加入ABCD四选项中的物质时,均能减小酸液的浓度,起到减缓反应速率的作用,但是当加入硫酸铜溶液时,由于金属铝比铜活泼,金属铝先与硫酸铜溶液发生如下反应:Fe+CuSO4═Cu+FeSO4,这样减少了与酸反应的金属铝的质量,从而影响到产生氢气的质量,与题目要求又不影响产生氢气的质量不符.故答案B不可行.
解答:A、加入适量的氯化钡溶液,尽管发生如下反应:BaCl2+H2SO4═BaSO4↓+2HCl 只是H+的浓度减小但质量不变,故反应速率减慢,又不影响氢气的质量,该措施可行.
B、加入适量的硫酸铜溶液,金属铝先与硫酸铜溶液发生如下反应:Fe+CuSO4═Cu+FeSO4,这样减少了与酸反应的金属铝的质量,从而影响到产生氢气的质量,故该措施不可行.
C、硫酸钠与硫酸和金属铝都不反应,加入适量的硫酸钠溶液后,只是增加了溶液的质量,降低了酸液的浓度,故能使反应速率减慢,又不影响氢气的质量,该措施可行.
D、加入适量的蒸馏水,稀释了酸液,故能使反应速率减慢,又不影响氢气的质量,该措施可行.
故选:B
点评:该题难度不大,但综合性较强,以影响反应速率的因素探究为情境,重点考查金属活动顺序的应用和对溶质质量分数的理解.

练习册系列答案
相关题目
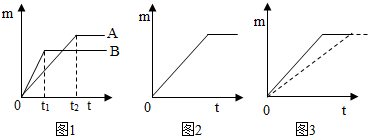
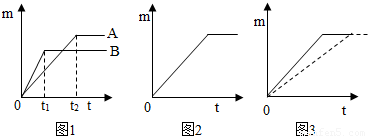
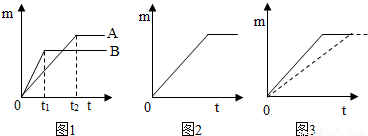
 (2007?常德)某同学为了研究影响金属与酸反应速率的因素,进行了一系列的探究实验.实验结果如图所示,图中每条斜线表示:该金属和对应酸的反应时间与生成氢气质量的关系.由图中的信息我们可以分析出影响金属与酸反应速率的因素有:
(2007?常德)某同学为了研究影响金属与酸反应速率的因素,进行了一系列的探究实验.实验结果如图所示,图中每条斜线表示:该金属和对应酸的反应时间与生成氢气质量的关系.由图中的信息我们可以分析出影响金属与酸反应速率的因素有: