题目内容
【题目】下面的表格中列出了氯化铵在不同温度下的溶解度:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
(1)从表中可得到的一条信息是;
(2)20℃时,向100g水中加入50g氯化铵,形成氯化铵的(填“饱和”或“不饱和”)溶液,将其温度升高至60℃时,所得溶液的质量为;
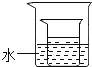
(3)将(2)中所得的60℃时的氯化铵溶液放入如图所示的小烧杯中,在大烧杯的水中加入下列物质,能够使小烧杯中有固体析出的是 (填字母序号);
A.冰
B.氯化钠
C.硝酸铵
D.氧化钙
(4)某同学欲配制20℃时20%的氯化铵溶液500g,需要氯化铵的质量 . 他在量取水时俯视读数,在其他操作都无误的情况下,他配制的溶液的溶质质量分数将(填“偏大”或“偏小”).
【答案】
(1)氯化铵的溶解度随温度升高而增大
(2)饱和;150克
(3)A,C
(4)100g;偏大
【解析】解:(1)从表中可以看出,温度越高,氯化铵的溶解度越大.故答案为:氯化铵的溶解度随温度升高而增大.(2)在20℃时,氯化铵的溶解度是37.2克.即向100g水中加入37.2g氯化铵恰好完全溶解.因此加入50克氯化铵,会形成饱和溶液,此时所得溶液的质量为150克.加入50克氯化铵后会完全溶解.故答案为:饱和;150克;(3)因为氯化铵的溶解度随温度的升高而增大,所以只要能使小烧杯中的温度降低的就可以使固体析出.即只要加到大烧杯中的物质能够吸热即可.A、冰融于水要吸热;B、氯化钠溶于水温度基本不变; C、硝酸铵溶于水要吸热; D、氧化钙溶于水要放热.
故答案为:AC;
(4)配制20℃时20%的氯化铵溶液500g,需要氯化铵的质量为:500g×20%=100g;用量筒量取水的体积时,俯视读数,读数比实际偏大,则会导致所量取水的实际体积小于所量的值,即所量取的水的实际体积偏小,溶剂的质量偏小,故所得溶液的质量分数偏大.
故答案为:100g;偏大.
(1)氯化铵的溶解度受温度影响;(2)在一定的温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液是饱和溶液;(3)根据氯化铵的溶解度随温度的降低而减小进行解答;(4)根据溶质质量分数的计算公式进行计算;根据量筒读数时的要求,视线要与量笥内液体凹液面的最低处保持水平,仰视液面,读数比实际偏小;俯视液面,读数比实际偏大;据此进行分析判断.

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案【题目】为测定锌铜合金中锌的含量,取该合金放入如图盛有稀硫酸的锥形瓶中.多次实验后,取平均值所得数据如表:
反应前 | 充分反应后装置及反应剩余物质质量 | |
装置和足量的稀硫酸质量 | 锌铜合金质量 | |
342.10g | 16.00g | 357.70g |
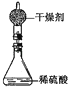
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)根据质量守恒定律求生成氢气的质量 .
(2)该合金中锌的质量分数.
