题目内容
【题目】为确定木炭还原氧化铜后的固体成分,请你与兴趣小组的同学完成以下探究。
【做出猜想】
猜想Ⅰ:全部是金属铜;
猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭;
猜想Ⅳ:除铜外,还含有氧化铜、木炭。
【设计实验】实验流程如图:
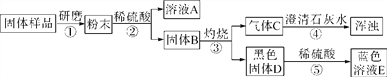
【问题和讨论】
(1)步骤②包括溶解、________两步操作;
(2)C的化学式为________,D的化学式为________,由此可以推出固体B中含有__________(写化学式);
(3)步骤④发生的反应方程式为______________________________;
(4)结合(2)的结论推断:如果溶液A显蓝色,则证明猜想________成立。
【答案】 过滤 CO2 CuO Cu、C CO2+Ca(OH)2===CaCO3↓+H2O Ⅳ
【解析】(1). 从实验流程图可知,操作②的目的是将难溶性固体与液体分离,所涉及步骤是溶解,过滤 ; (2). 氧化铜能与硫酸反应生成易溶于水的硫酸铜和水,由题中信息可知操作②所得固体成分铜或铜与木炭的混合物,灼烧时碳和氧气反应生成CO2 ; (3).灼烧时,铜与氧气反应生成 CuO,(4). 澄清石灰水变浑浊证明有二氧化碳生成,说明固体中有碳,加硫酸后得蓝色溶液,说明D中有氧化铜和硫酸反应生成蓝色的硫酸铜溶液,证明B中有铜;即B是Cu、C混合物; (5). 二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应方程式为:CO2+Ca(OH)2===CaCO3↓+H2O ; (6). 如果溶液A显蓝色,则证明粉末中有氧化铜,猜想Ⅳ成立。
点睛:熟练掌握碳和氧化铜,氧化铜与硫酸等的反应,及二氧化碳的验证,硫酸铜溶液的颜色。

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目