题目内容
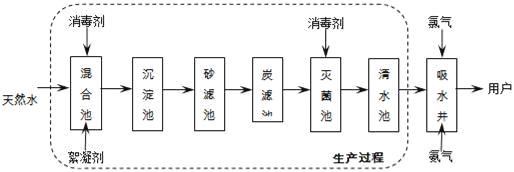
【题目】某班同学用如图装置测定空气里氧气的含量。先用弹簧夹夹住乳胶管。点燃红磷,伸入瓶中并塞上瓶塞。待红磷熄灭后一段时间,打开弹簧夹,观察广口瓶内水面变化情况。实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5, 下列对这种现象解释不合理的是( )

A. 甲同学使用红磷的量太少,瓶内氧气没有消耗完
B. 甲同学未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
C. 甲同学未等到冷却至室温就打开弹簧夹
D. 甲同学插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出
【答案】D
【解析】A、实验中所取红磷的量不足,会使装置内氧气不能被全部消耗,所以使得广口瓶内水面上升明显小于瓶内体积的五分之一,故解释合理;B、若甲同学可能未塞紧瓶塞,则会使实验装置漏气,那么外界空气就会进入集气瓶内,因此测得氧气的体积分数小于五分之一,故解释合理;C、甲同学未等到冷却至室温就打开弹簧夹,会导致实验中装置内的气体受热膨胀而逸出,所以使得广口瓶内水面上升明显小于瓶内体积的五分之一,故解释合理;D、甲同学插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出,因此测定氧气体积分数增大,故D解释不合理;故选D。

 初中暑期衔接系列答案
初中暑期衔接系列答案【题目】定量和定性研究对于化学科学发展有重大作用,请回答下列问题。
(1)二氧化锰对过氧化氢的分解有催化作用,现将34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开。不同时间电子天平的读数如下表所示(不考虑H2O逸出):
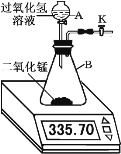
反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
装置 + 过氧化氢溶液 + 二氧化锰/g | 335.70 | 333.78 | 332.64 | 332.58 | 332.50 | 332.50 | 332.50 |
由题目可知产生氧气的质量为__________
根据上述氧气的量计算参加反应的过氧化氢的物质的量(根据化学方程式列式计算)________
(2)小明同学发现FeCl3溶液和CuSO4溶液对过氧化氢的分解也有催化作用,为比较相同浓度的FeCl3溶液和CuSO4溶液对过氧化氢分解的催化效果,他进行了如下探究:
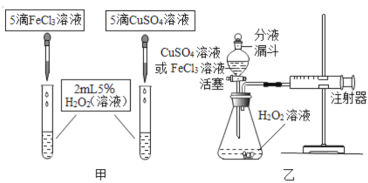
(定性探究)
如图甲,可通过观察_______来定性比较两者的催化效果。此时对比实验应控制的相同条件是____________。
(定量研究)
如图乙,要定量比较两者的催化效果,可测量生成等体积所需的_________;实验前要做的是___________。