题目内容
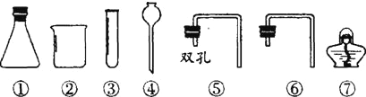
【题目】下列装置常用于实验室制取气体。请根据给出的装置回答下列问题。
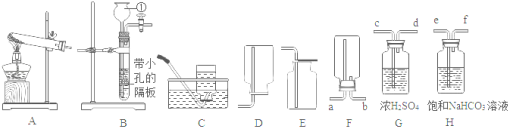
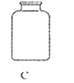
(1)写出仪器①的名称_____。
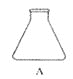
(2)实验室用氯酸钾制取氧气,应选用的发生装置是_____(填序号),化学方程式是_____,若用C装置收集氧气,当观察到_____时,开始收集。
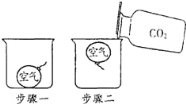
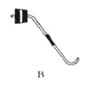
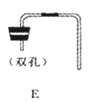
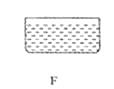
(3)用B和E装置制取并收集CO2,反应的化学方程式为_____。选择装置B作为制取CO2气体的发生装置,其突出优点是_____,若改用F装置收集二氧化碳,则气体应从____(填“a”或“b”)端进入。制得的二氧化碳中常含有少量的氯化氢气体和水蒸气,欲使用G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→_____(用导气管端口字母表示)
【答案】长颈漏斗A2KClO3![]() 2KCl + 3O2 ↑气泡均匀连续的放出CaCO3+2HCl==CaCl2+H2O+CO2↑可以控制反应的发生和停止befcd
2KCl + 3O2 ↑气泡均匀连续的放出CaCO3+2HCl==CaCl2+H2O+CO2↑可以控制反应的发生和停止befcd
【解析】
根据用氯酸钾制氧气、实验室制二氧化碳原理,操作方法进行分析解答。
(1)仪器①的名称为长颈漏斗;
(2)如果用氯酸钾制氧气,氯酸钾是固体且需要加热,应选用装置A,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,该反应的化学方程式是2KClO3![]() 2KCl + 3O2 ↑;若用C装置收集氧气,若一有气泡就收集,得到的气体混有空气,为了得到较纯的氧气,当观察到:气泡均匀连续的放出时,开始收集;
2KCl + 3O2 ↑;若用C装置收集氧气,若一有气泡就收集,得到的气体混有空气,为了得到较纯的氧气,当观察到:气泡均匀连续的放出时,开始收集;
(3)实验室制取CO2,是在常温下,用大理石(或石灰石)和稀盐酸制取的,大理石(或石灰石)的主要成分是碳酸钙,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,该反应的化学方程式是CaCO3+2HCl==CaCl2+H2O+CO2↑;选择装置B作为制取CO2气体的发生装置时,大理石(或石灰石)放在多孔隔板上,盐酸从长颈漏斗中加入,关闭开关时,试管中的气体增多,压强增大,把盐酸压入长颈漏斗,大理石(或石灰石)和盐酸分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,大理石(或石灰石)和盐酸混合,反应进行,所以选择装置B作为制取CO2气体的发生装置,其突出优点是:可以控制反应的发生和停止;二氧化碳的密度比空气大,若改用F装置收集二氧化碳,则气体应从b进入;制得的二氧化碳中常含有少量的氯化氢气体和水蒸气,碳酸氢钠与盐酸反应生成物氯化钠、水和二氧化碳,碳酸氢钠溶液可除去氯化氢气体,浓硫酸具有吸水性,可除去水蒸气,要先除杂质后干燥,并且长进短出,所以欲使用G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→efcd。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案