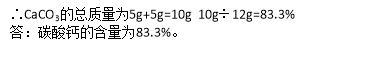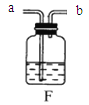题目内容
【题目】(8分)同学们对实验“煅烧石灰石”展开深入探究。
资料:石灰石中的杂质高温不分解且不与稀盐酸反应
(1)为证明石灰石已分解,三位同学设计方案如下:
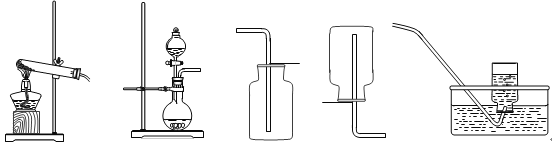
Ⅰ.甲同学按图一所示进行实验(煤气灯亦能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式 。
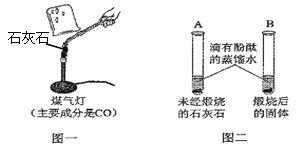
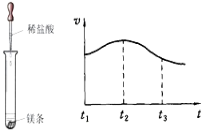
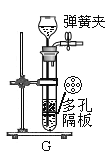
II.乙同学按图二所示进行试验,观察到B中液体变 色,A实验的作用 。
III.丙同学取一块质量为12g的石灰石煅烧,一段时间后发现固体质量减轻2.2g,证明石灰石已分解。
IV.大家认为甲同学的方案不合理,请分析原因 。
(2)为测定石灰石的纯度,丙同学将他刚才煅烧后的固体放入足量稀盐酸中,又产生2.2g气体,结合上述数据计算:丙所取的这块石灰石中碳酸钙的质量分数是多少?
计算过程写在答卷上
【答案】(1)ⅠCO2+Ca(OH)2=CaCO3↓+H2O Ⅱ 红 对比 Ⅳ CO燃烧会产生CO2
(2)83.3%
【解析】
试题分析:(1) Ⅰ、烧杯内壁石灰水变浑浊,发生的化学反应方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,
Ⅱ、乙同学按图二所示进行试验,未煅烧的石灰石不溶于水,煅烧后生成了氧化钙,氧化钙和水发生反应,生成了氢氧化钙,水溶液呈碱性,所以滴入酚酞的蒸馏水后,液体变为红色,A实验的作用对比
IV、甲同学的方案不合理的原因是:煤气灯的燃料是一氧化碳,而CO燃烧会产生CO2
(2) 根据反应:CaCO3![]() CaO+CO2↑,丙同学取一块质量为12g的石灰石煅烧,一段时间后发现固体质量减轻2.2g,说明该反应生成了2.2g二氧化碳,这样便可计算出发生分解的碳酸钙质量,丙同学将他刚才煅烧后的固体放入足量稀盐酸中,又产生2.2g气体,说明发生了反应:CaCO3+2HCl==CaCl2+H2O+CO2↑,这样同样可以计算出剩余碳酸钙的质量
CaO+CO2↑,丙同学取一块质量为12g的石灰石煅烧,一段时间后发现固体质量减轻2.2g,说明该反应生成了2.2g二氧化碳,这样便可计算出发生分解的碳酸钙质量,丙同学将他刚才煅烧后的固体放入足量稀盐酸中,又产生2.2g气体,说明发生了反应:CaCO3+2HCl==CaCl2+H2O+CO2↑,这样同样可以计算出剩余碳酸钙的质量
解:设加热分解的碳酸钙的质量为x
CaCO3![]() CaO+CO2↑
CaO+CO2↑
100 44
x 2.2g
100:44=x:2.2g x=5g
设剩余碳酸钙的质量为y
CaCO3+2HCl==CaCl2+H2O+CO2↑
100 44
y 2.2g
100:44=y:2.2g y=5g