题目内容
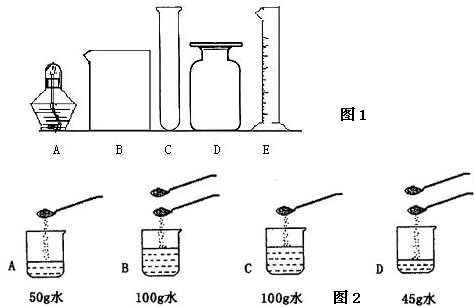
在实验室配制溶液时,常涉及以下过程:①溶解②称量③计算④装瓶存放.请按要求回答问题:(1)现欲配制50g 5%氯化钠溶液,配制过程的先后顺序是
(2)用已调节平衡的天平称取氯化钠固体时,发现指针偏右,接下来的操作是
(3)在量取蒸馏水体积时,若仰视读数,则会导致氯化钠溶液的溶质质量分
数
(4)在溶解步骤中需要的仪器有
(5)配制100克质量分数为20%的稀硫酸,需要质量分数为98%的浓硫酸
分析:(1)对配制溶液的过程进行排序;
(2)分析称量操作,完成对固体药品的称量;
(3)分析没正确使用量筒对配制溶液结果的影响;
(4)写出溶解过程所需要的仪器;
(5)根据加水稀释溶液前后溶质质量不变,计算配制一定量稀硫酸所需浓硫酸的质量.
(2)分析称量操作,完成对固体药品的称量;
(3)分析没正确使用量筒对配制溶液结果的影响;
(4)写出溶解过程所需要的仪器;
(5)根据加水稀释溶液前后溶质质量不变,计算配制一定量稀硫酸所需浓硫酸的质量.
解答:解:(1)用固体药品食盐配制溶液时的操作步骤为:计算-称量-溶解-装瓶存放;
故答案为:③②①④(1分)
(2)天平指针偏向右边,说明右盘的砝码质量大于左盘食盐质量,因此还需要再加入食盐至天平平衡;
故答案为:继续添加药品直至天平平衡(1分)
(3)仰视读数时,由于视线低于液面,所以所读数值小于实际体积,即所量取水的体积偏大,因此所配制溶液的质量分数偏小;
故答案为:<(1分)
(4)溶解需要在烧杯内进行,为加快食盐的溶解需要使用玻璃棒不断搅拌,直到固体全部溶解;
故答案为:烧杯(1分)、玻璃棒(1分)
(5)需要质量分数为98%的浓硫酸的质量=
≈20.2g
故答案为:20.2(2分)
故答案为:③②①④(1分)
(2)天平指针偏向右边,说明右盘的砝码质量大于左盘食盐质量,因此还需要再加入食盐至天平平衡;
故答案为:继续添加药品直至天平平衡(1分)
(3)仰视读数时,由于视线低于液面,所以所读数值小于实际体积,即所量取水的体积偏大,因此所配制溶液的质量分数偏小;
故答案为:<(1分)
(4)溶解需要在烧杯内进行,为加快食盐的溶解需要使用玻璃棒不断搅拌,直到固体全部溶解;
故答案为:烧杯(1分)、玻璃棒(1分)
(5)需要质量分数为98%的浓硫酸的质量=
| 100g×20% |
| 98% |
故答案为:20.2(2分)
点评:量筒量取液体时,视线应与液体凹液面最低点在同一水平面上;视线低于液面称为仰视,所读体积偏小;视线高于液面称为俯视,读数偏大.

练习册系列答案
相关题目