题目内容
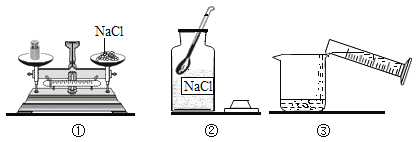
【题目】(1)下图为实验室制取并收集气体的装置图,回答下列问题。
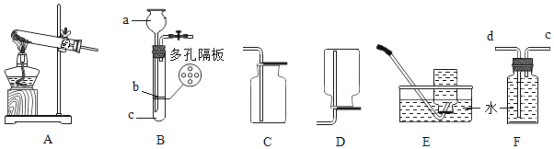
①a仪器的名称是___________。
②实验室用高锰酸钾制取并收集干燥的氧气应选用的装置组合是________(填序号)。
③若用F装置收集并测量氧气的体积,应在________(填“d”或“e”)段连接量筒。
④实验室制取二氧化碳的化学方程式是_________,用B装置制取二氧化碳便于控制反应的发生与停止,制取时应将大理石放在________(填“b”或“c”)。
(2)某化学兴趣小组在学完金属活动性顺序相关知识后,他们做了钠与硫酸铜溶液反应的实验,发现并没有铜生成,而是产生蓝色沉淀和少量黑色物质。于是他们进行了如下探究:
(实验探究1)取一块绿豆大小的金属钠,放入盛有20mL蒸馏水的烧杯中,发现金属钠浮在水面上,熔化成一个闪亮的小球并四处游动,发出嘶嘶的响声,收集反应产生的气体,发现该气体能燃烧。
(实验探究2)在上述反应所得溶液中滴加硫酸铜溶液,产生蓝色絮状沉淀。
(实验探究3)将蓝色絮状沉淀加热得到黑色固体。
(查阅资料)①钠在常温下能与水剧烈反应,生成一种碱和一种气体。②氢氧化铜受热易分解。③氧化铜为黑色固体。
(问题分析)①写出钠与水反应的化学方程式___________,点燃反应产生的气体前一个先____________。
②写出产生蓝色絮状沉淀的化学方程式____________。
(实验结论)在金属活动性顺序中,活动性较强的金属____________(填“一定”或“不一定”)能将位于其后面的金属从它们的盐溶液中置换出来。
(反思与交流)钠与硫酸铜溶液反应产生少量黑色物质的可能原因是____________。
【答案】长颈漏斗 AC d CaCO3+2HCl=CaCl2+H2O+CO2↑ b 2Na +2H2O=2NaOH +H2↑ 验纯 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 不一定 钠与水反应放出热量,氢氧化铜受热分解产生氧化铜
【解析】
(1)由图可知①a仪器的名称是长颈漏斗,故填:长颈漏斗。
(2)②实验室用高锰酸钾制取并收集干燥的氧气该反应需加热,故发生装置选A,氧气密度比空气大收集干燥的氧气可以用向上排空气法收集,收集装置选C,故选:AC。
(3)③若用F装置收集并测量氧气的体积,氧气密度小于水的密度,气体短进长出,e进d出,应在d端连接量筒,故选:d。
(4)④实验室用石灰石或大理石和稀盐酸制取二氧化碳,化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,用B装置制取二氧化碳便于控制反应的发生与停止,在装置B中,固体药品放在多孔隔板上,液体药品从长颈漏斗中加入。反应开始后,关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行,故填:CaCO3+2HCl=CaCl2+H2O+CO2↑,b。
(5)钠与水反应,常温下生成一种碱和一种气体,故可推测生成氢氧化钠和氢气,化学方程式为2Na +2H2O=2NaOH +H2↑,氢气和空气容易形成爆炸性混合物,故点燃前需要验纯,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,故填:2Na +2H2O=2NaOH +H2↑;验纯;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4。
(6)活动性非常强的金属会先和水反应,故在金属活动性顺序中,活动性较强的金属不一定能将位于其后面的金属从它们的盐溶液中置换出来,故填:不一定。
(7)氢氧化铜受热易分解生成氧化铜,氧化铜为黑色固体,钠与硫酸铜溶液反应产生少量黑色物质的可能原因是钠与水反应放出热量,氢氧化铜受热分解产生氧化铜,故填:钠与水反应放出热量,氢氧化铜受热分解产生氧化铜。

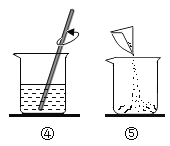
【题目】(1)从下图中选择合适的仪器,组装成制取氧气的发生装置,且能够随时添加药品,所选仪器应是_______(填序号)。适用于这种装置制取氧气的化学方程式为_______。
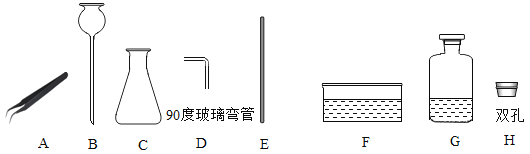
(2)生活中,有许多物品的使用与实验室中仪器的作用相似。请在上图中选择作用相似的仪器,将其名称填入下表中对应的位置。
生活物品 | 物品的使用 | 作用相似的仪器名称 |
酒瓶 | 盛放白酒 | ____ |
洗脸盆 | 盛放清水 | ____ |
两根筷子 | 夹取盘中的青菜 | ____ |
一根筷子 | 水中放入白糖,搅拌 | ____ |
【题目】a、b是常见的两种固体物质,根据图表的信息回答下列问题:
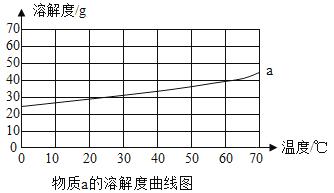
物质b的溶解度表
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
b的溶解度/g | 14 | 20 | 30 | 45 | 65 | 85 | 110 |
(1)60℃时,物质a的溶解度是______g。
(2)20℃时,将20g物质b加入到50g水中,充分溶解后得到溶液的质量为________g。
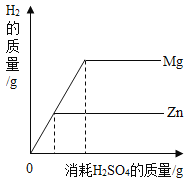
(3)将50℃时a、b两物质的饱和溶液分别降温至20℃,所得溶液的溶质质量分数大小关系为a______b(填“>”、“=”或者“<”)。
(4)下列说法正确的组合是_______(填字母序号)。
①所有物质的溶解度都随温度的升高面增大
②30℃时,物质的溶解度a小于b
③物质b中含有少量a时,可以采用降温结晶的方法提纯b
④40℃时,分别将物质a、b的饱和溶液降温至10℃,析出物质的质量b大于a
A ①④
B ①③
C ②③
D ②④