题目内容
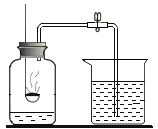
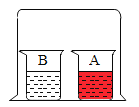
【题目】根据如图所示装置回答有关问题:
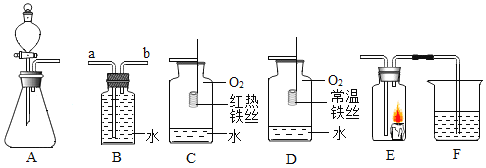
(1)若用装置B排水收集氧气,气体从_____(填“a”或“b”)导管通入瓶内。进行装置C中的实验时瓶底留少量水的作用是______。红热的铁丝在空气中不易燃烧而能够在氧气中剧烈燃烧的微观原因是_______。
(2)对比装置D和C,可以得出关于可燃物燃烧的条件是_______。
(3)某同学连接A、E、F进行实验,A中所加药品不同,F中所加药品相同。
①若实验时E中蜡烛熄灭,F中溶液变浑浊。F中溶液变浑浊的化学方程式为_____________。
②若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则A中反应的化学方程式为____________。
(4)某同学为探究二氧化碳的性质,进行如下操作:
①向一个收集满二氧化碳气体的软质塑料瓶甲中加人约三分之一体积的水,立即紧瓶盖,振荡,产生的现象是________,说明二氧化碳的性质是__________。
②取3mL瓶甲中的液体倒入试管乙中,滴加紫色石蒸试液,振荡观察到溶液变__色,说明二氧化碳与水发生化学反应,化学方程式为______________。
【答案】b 防止生成的熔化物溅落下来,炸裂瓶底 单位体积的空间里氧分子的数目越多,这些物质与氧气分子接触和碰撞的机会就越多,反应就越剧烈 温度要达到着火点 CO2+Ca(OH)2═CaCO3↓+H2O 2H2O2![]() 2H2O+O2↑ 软塑料瓶变瘪 二氧化碳溶于水 红
2H2O+O2↑ 软塑料瓶变瘪 二氧化碳溶于水 红 ![]()
【解析】
(1)氧气的密度比水小,气体从b通入,水从a排出;铁丝燃烧时瓶底留少量水是防止生成的熔化物溅落下来,炸裂瓶底;氧气具有助燃性,可燃物在氧气中燃烧比在空气中剧烈,从微观的角度分析,是因为单位体积的空间里氧分子的数目越多,这些物质与氧气分子接触和碰撞的机会就越多,反应就越剧烈;
(2)C中红热的铁丝能燃烧,D中常温下的铁丝不燃烧,可以得出可燃物燃烧必须达到着火点;
(3)①F中溶液变浑浊是二氧化碳与石灰水的反应,化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O;
②实验时E中蜡烛燃烧更旺,说明生成的气体是氧气,过氧化氢溶液在二氧化锰做催化剂的条件下生成水和氧气,则A中反应的化学方程式为2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(4)①向集满二氧化碳气体的软塑料瓶中加入约三分之一体积的水,立即旋紧瓶盖,振荡,观察到的现象是:软塑料瓶变瘪;因为二氧化碳溶于水,瓶内气体压强减小,小于外界大气压的缘故;
②二氧化碳与水反应生成了碳酸,碳酸能使紫色的石蕊试液变红色;反应的化学方程式为:![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
下列判断正确的是
A.表中a的值为5.6 B.X可能是该反应的催化剂
C.X可能含有氢元素 D.X只含碳元素
【题目】鸡蛋壳中含有碳酸钙,为了测定蛋壳中碳酸钙的质量分数,某兴趣小组取鸡蛋壳和足量稀盐酸在烧杯中反应(假设蛋壳中杂质不与稀盐酸反应,反应产生气体全部放出),有关实验数据如下表:
反应前反应后 | |||
实验数据 | 鸡蛋壳质量 | 烧杯和稀盐酸质量 | 烧杯和其中混合物的质量 |
12g | 120g | 127.6 g |
试计算:
(1)生成二氧化碳的质量是多少g。
(2)计算鸡蛋壳中碳酸钙的质量分数(写出计算过程,计算结果保留一位小数)。