题目内容
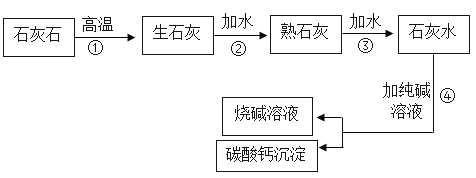
【题目】工业上用纯碱(Na2CO3)和石灰石为原料制备烧碱的简要工艺流程如图所示,请回答。
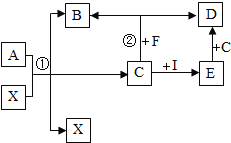
(1)石灰石、生石灰、熟石灰均能与下列____(填字母)发生化学反应。
A水 B盐酸 C二氧化碳
(2)将最后所得的烧碱溶液和碳酸钙沉淀分离,可用______(操作名称)将它们分离。
(3)化学反应②的基本反应类型属于______反应。
【答案】B 过滤 化合
【解析】
氧化钙能和水反应生成氢氧化钙,盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,盐酸和氢氧化钙反应生成氯化钙和水,氧化钙和盐酸反应生成氯化钙和水,二氧化碳和氢氧化钙反应生成碳酸钙和水。
(1)A、石灰石的主要成分是碳酸钙,生石灰是氧化钙,熟石灰是氢氧化钙,其中氧化钙能和水反应,碳酸钙和氢氧化钙不和水反应,故A不正确;
B、盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,盐酸和氢氧化钙反应生成氯化钙和水,氧化钙和盐酸反应生成氯化钙和水,故B正确;
C、二氧化碳和氢氧化钙反应生成碳酸钙和水,和碳酸钙、氧化钙均不反应,故C不正确。故选B。
(2)过滤可将固体和液体分离,故将最后所得的烧碱溶液和碳酸钙沉淀分离,可用过滤将它们分离。
(3)化学反应②是氧化钙和水反应生成氢氧化钙,反应符合多变一,故基本反应类型属于化合反应。

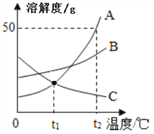
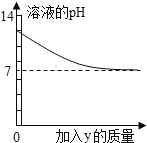
【题目】烧杯中盛有 x 溶液,逐滴加入(或通入)y 物质,烧杯内液体的 pH 变化如下图所示。则符合该变化的一组物质是
x | y | |
A | NaOH 溶液 | 稀 HCl(过量) |
B | 稀 H2SO4 | Mg(适量) |
C | Ca(OH)2 | CO2(适量) |
D | 稀 HCl | NaOH 溶液(过量) |
A.AB.BC.CD.D
【题目】Mg(OH)2是一种新型的阻燃剂,在温度达到380°C时吸收热量并分解产生水,同时生成的氧化镁附着于可燃物的表面阻止了进一步燃烧。
(1)Mg(OH)2 受热分解化学方程式是________________;工业常用氯化镁溶液与烧碱溶液制取Mg(OH)2,化学方程式是___________________。
(2)某同学用氨水在实验室模拟制取Mg(OH)2的过程:一定温度下,往含一定量氯化镁的溶液中加入适量氨水( 氨水易挥发),再经过滤、洗涤得到Mg(OH)2晶体。为探究获得较高Mg(OH)2晶体转化率条件,该同学进行如下对比实验,数据如下:
实验编号 | 氯化镁溶液溶质质量分数 | 反应温度/°C | Mg(OH)2转化率/% |
a | 10% | 30 | 27.06 |
b | 15% | 30 | 56.77 |
c | 15% | 40 | 69.64 |
d | 15% | 60 | 54.30 |
e | 20% | 60 | 50.60 |
①实验b和c的目的是______________________。
②由实验可知,能够得到最多Mg(OH)2的条件是溶质质量分数_______和温度__________°C。
③在氯化镁溶液溶质质量分数都是15%的情况下,60°C 时Mg(OH)2的转化率比40°C时低的原因是________________。
(3)根据燃烧的条件可知,Mg(OH)2能做阻燃剂的原因是________________(填编号)。
①清除可燃物 ②使温度 降低到着火点以下 ③隔绝空气
(4)氯化镁溶液通过循环利用,理论上转化率可以达到100%。若生产了2.9吨Mg(OH)2,理论上需要原料20%的氯化镁溶液_______________吨。