题目内容
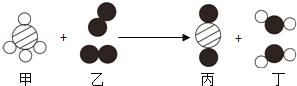
【题目】某化学兴趣小组用下列流程模拟用一氧化碳还原氧化铜制取铜的过程。

(1)木炭、氧化铜要研磨成粉末状的原因是______________。
(2)你认为通入的气体速度快好或是慢好_____________。
(3)丙中产生的现象为_____________,发生的反应的化学方程式为_____________,丙中生成物中可以循环的物质的化学式为_______。
(4)乙中发生反应的化学方程式为__________________ 。
(5)尾气不经过处理能否直接排放到空气中________(填“能”或“否”),原因是____________。
【答案】加快反应速率,使反应更充分 慢 黑色粉末变红 CuO+CO![]() Cu+CO2 CO2 CO2+C
Cu+CO2 CO2 CO2+C![]() 2CO 否 CO气体有毒,排放到空气中会污染环境
2CO 否 CO气体有毒,排放到空气中会污染环境
【解析】
(1)反应物的接触面积越大,反应速率越快。把木炭和氧化铜要研磨成粉末状能加快反应速率,使反应更充分;
(2)通入的气体速度还是慢好,便于反应充分进行;
(3)一氧化碳与氧化铜反应生成铜和二氧化碳,所以丙装置中可看到黑色粉末变红,其反应方程式为:CuO+CO![]() Cu+CO2;尾气中的二氧化碳再与碳反应又有CO产生,CO可作为前面的反应(丙)中的反应物,所以丙中生成物中可以循环的物质是二氧化碳,化学式为:CO2;
Cu+CO2;尾气中的二氧化碳再与碳反应又有CO产生,CO可作为前面的反应(丙)中的反应物,所以丙中生成物中可以循环的物质是二氧化碳,化学式为:CO2;
(4)在高温条件下,碳与二氧化碳反应生成了一氧化碳:CO2+C![]() 2CO;
2CO;
(5)因为CO气体有毒,排放到空气中会污染环境,所以不能把CO排放到空气中。

【题目】某密闭容器内有X、Y、Z、W四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 | X | Y | Z | W |
反应前质量 | 4 | 1 | 10 | 2 |
反应后质量 | 待测 | 5 | 4 | 8 |
下列说法正确的是![]()
![]()
A. 反应后X的质量为8g
B. Z与W的相对分子质量比一定是1:1
C. 该反应的反应物只有Z
D. 参加反应的X与Z的质量比是2:3