题目内容
用氯化钠和碳酸氢铵(NH4HCO3)可制备碳酸氢钠和氯化铵(NH4CL),该反应可表示为:NaCl+NH4HCO3═NaHCO3+NH4Cl.
资料:20℃时四种物质的溶解度如下,(假设它们同时溶解在水中各自的溶解度不变).
(1)20℃时,20克氯化钠放入50克的水中,充分搅拌形成溶液是
(2)20℃时,等质量四种物质的饱和溶液中溶剂质量最大的是
(3)20℃时,按上述化学方程式中反应物的质量比,向100g水中加入11.7gNaCl和15.8gNaHCO3.理论上从溶液中析出晶体的质量为
资料:20℃时四种物质的溶解度如下,(假设它们同时溶解在水中各自的溶解度不变).
| 物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 |
| 溶液度/g | 36.0 | 21.6 | 37.2 | 9.6 |
饱和
饱和
(饱和、不饱和溶液),溶质和溶剂的质量比是9:25
9:25
.(2)20℃时,等质量四种物质的饱和溶液中溶剂质量最大的是
NaHCO3
NaHCO3
.(3)20℃时,按上述化学方程式中反应物的质量比,向100g水中加入11.7gNaCl和15.8gNaHCO3.理论上从溶液中析出晶体的质量为
6.2
6.2
g,晶体的名称是碳酸氢钠
碳酸氢钠
.分析:(1)根据20℃时,氯化钠的溶解度考虑;(2)20℃时,等质量四种物质的饱和溶液中溶剂质量最大的是溶解度最小的物质;(3)根据20℃时,NaCl和NaHCO3的溶解度考虑.
解答:解:(1)20℃时,氯化钠的溶解度是36.0g,即100g水中最多溶解36g氯化钠,所以该温度下,50g水中最多溶解18g,所以20℃时,20克氯化钠放入50克的水中,充分搅拌形成溶液是饱和溶液,且有2g没溶解,溶质和溶剂的质量比是:18g:50g=9:25;
(2)20℃时,等质量四种物质的饱和溶液中溶剂质量最大的是溶解度最小的物质,由图表数据可知碳酸氢钠溶解度最小;
(3)20℃时,NaCl的溶解度是36.0g,所以100g水中最多溶解36.0g氯化钠,所以向100g水中加入11.7gNaCl不会析出晶体;20℃时,NaHCO3的溶解度是9.6g,即该温度下,100g水中最多溶解9.6g碳酸氢钠,所以向100g水中加入15.8gNaHCO3,只能溶解9.6g,析出晶体质量为:15.8g-9.6g=6.2g,析出的晶体是碳酸氢钠.
故答案为:(1)饱和;9:25;(2)NaHCO3;(3)6.2g;碳酸氢钠.
(2)20℃时,等质量四种物质的饱和溶液中溶剂质量最大的是溶解度最小的物质,由图表数据可知碳酸氢钠溶解度最小;
(3)20℃时,NaCl的溶解度是36.0g,所以100g水中最多溶解36.0g氯化钠,所以向100g水中加入11.7gNaCl不会析出晶体;20℃时,NaHCO3的溶解度是9.6g,即该温度下,100g水中最多溶解9.6g碳酸氢钠,所以向100g水中加入15.8gNaHCO3,只能溶解9.6g,析出晶体质量为:15.8g-9.6g=6.2g,析出的晶体是碳酸氢钠.
故答案为:(1)饱和;9:25;(2)NaHCO3;(3)6.2g;碳酸氢钠.
点评:解答本题关键是要熟记溶解度的四要素,并能灵活运用解决实际问题.

练习册系列答案
相关题目
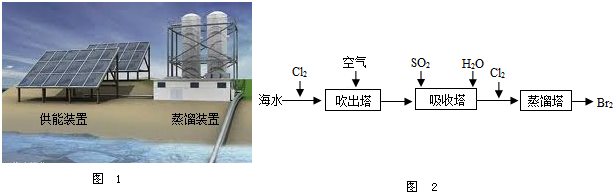
 (2012?北京)海洋为人类提供了宝贵的自然资源.
(2012?北京)海洋为人类提供了宝贵的自然资源.