题目内容
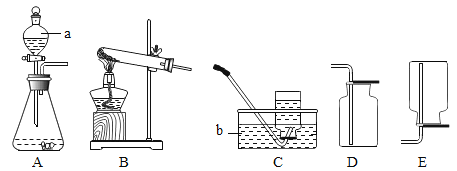
【题目】亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2。N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3,如图为制取少量NH3的装置(制取H2的装置已略去)
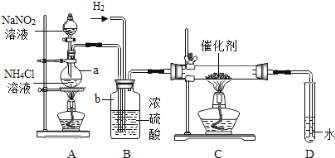
(1)写出a、b两种仪器的名称:a:_____b:_______
(2)为了获得较纯净的氢气,该实验中制取氢气的化学方程式最好是________。
(3)写出C装置的硬质试管中发生反应的化学方程式_______
(4)反应时N2和H2的最佳质量比是___________.如果按此比例进行反应,反应时D中导管口是否会出气泡_______?(已知NH3极易溶于水),说明逸出气泡的原因_______
(5)B装置的作用除了将两种气体混合外,还有_________________、
(6)结合本实验装置,证明确实有NH3生成的简单方法及实验现象是_______
(7)归纳与演绎是重要科学方法,也是常用的学习方法,我们已经学过实验室制取气体的反应原理、制取与收集方法请你归纳出实验室制取气体反应的共同点;________(填序号).
①需要加热 ②使用催化剂 ③没有气体参加反应 ④原料为纯净物 ⑤只生成一种气体
【答案】烧瓶 广口瓶 Zn+H2SO4=ZnSO4+H2↑ N2+3H2![]() 2NH3 14:3 是 因为N2 在一定条件下能与H2部分化合生成NH3,仍会有未反应的N2与H2,且N2与H2难溶于水,所以未反应的N2与H2逸出 干燥氢气和氮气的作用 向D中滴加无色酚酞试液,溶液由无色变为红色 ③⑤
2NH3 14:3 是 因为N2 在一定条件下能与H2部分化合生成NH3,仍会有未反应的N2与H2,且N2与H2难溶于水,所以未反应的N2与H2逸出 干燥氢气和氮气的作用 向D中滴加无色酚酞试液,溶液由无色变为红色 ③⑤
【解析】
(1)a是烧瓶,b是广口瓶。
(2)用稀盐酸制取的氢气中混有水蒸气,要获得较纯净的氢气,选用稀硫酸,选用的金属是锌,锌与稀硫酸的反应速率适中,化学方程式为:Zn+H2SO4=ZnSO4+H2↑。
(3)根据题给信息,C装置中是氮气与氢气发生化学反应,反应的化学方程式为:N2+3H2![]() 2NH3,反应中,N2与H2的质量比是28:6=14:3。会有气泡逸出,因为N2 在一定条件下能与H2部分化合生成NH3,仍会有未反应的N2与H2,且N2与H2难溶于水,所以未反应的N2与H2逸出。
2NH3,反应中,N2与H2的质量比是28:6=14:3。会有气泡逸出,因为N2 在一定条件下能与H2部分化合生成NH3,仍会有未反应的N2与H2,且N2与H2难溶于水,所以未反应的N2与H2逸出。
(5)浓硫酸具有吸水性,能干燥气体,所以B装置的作用除了将两种气体混合外,还有干燥氢气和氮气的作用。
(6)向D中加入无色酚酞试液,酚酞试液变红,说明D中有显碱性的溶液,进一步证明氢气和氮气反应生成了氨气(氨气溶于水是氨水,氨水显碱性)。
(7)实验室制取气体时,应考虑产生的气体易收集、收集的气体较纯净等因素,所以反应的共同点是:没有气体参加反应且只生成一种气体。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案【题目】小明家新楼房刚修好。准备用石灰浆刷墙。石灰浆是用生石灰与水充分搅拌形成糊状物。工人师傅将石灰浆糊在墙上推平整。开始墙面很软,慢慢地会自然变干变硬。有一天小明回家,发现刚糊好的墙面掉下一块白色固体。准备通过实验来研究该固体的成分,请你参与。
(猜想)固体可能是A:生石灰,B:_________ ,C:___________。D:熟石灰和石灰石。
小明经过分析认为A是不可能的。请你用方程式解释___________。
(实验)小明取少量固体研细,加入一定量蒸馏水搅拌,澄清。
操作方法 | 现象 | 结论 |
取上层清液少许,滴入1-2滴无色酚酞试液 | 无现象 | 猜想____ 不正确 |
小明另取少量固体于试管,注入___________发现有气泡。故猜想__________成立。
(反思)产生气泡的原因(方程式)______________。
【题目】马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如表所示:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
生成气体的总质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
试求:
(1)m的值为_____g。
(2)12g石灰石样品中碳酸钙的质量_____?
(3)所用稀盐酸溶液中溶质的质量分数_____?
(4)反应完全后最终溶液中氯化钙的质量分数_____?(结果保留小数点后一位小数)
【题目】科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环(如图1所示)。
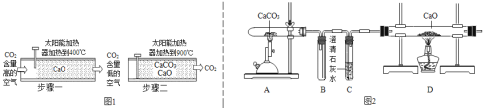
某化学小组的同学对此非常感兴趣,在老师的指导下,设计如图2所示的装置探究上述设想的反应原理是否可行。
⑴能证明装置A“释放CO2”的现象是_____;
⑵装置B的作用是_____;
⑶上述反应结束后,小组同学对D中固体的成分进行探究,以证明是否“捕捉”到CO2。
(猜想与假设)D中的固体可能为:I.只有氧化钙;Ⅱ.氧化钙和碳酸钙;Ⅲ.只有碳酸钙
(进行实验)
①甲同学从D中取一定量的固体于试管中,并加入少量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立。乙同学认为上述实验不足以证明猜想Ⅲ成立,其理由是_____。
②乙同学从D中取一定量的固体于试管中,加入少量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生。乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。丙同学认为乙的实验不足以证明猜想I成立,理由是_____。
③丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅱ成立,请完成他的实验报告。
实验步骤 | 实验现象 | 实验结论 | |
取样,加入适量的水溶解,过滤 | 向滤液中加入_____ | _____ | 猜想Ⅱ成立 |
向滤渣中加入_____ | _____ | ||
⑷通过以上探究,小组同学认为科学家的设想在反应原理上是可行的。该设想的优点有_____(填字母序号)。
A原料易得 B 充分利用太阳能 C 释放出的CO2可作为资源加以利用