题目内容
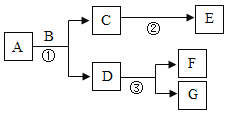
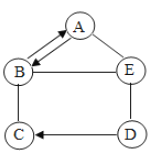
【题目】已知A、B、C、D、E分别为氧化铜、硫酸、氢氧化钠、硫酸铜和碳酸钠中的一种,它们之间的反应或转化关系如图(部分物质和反应条件已略去),已知C的溶液显蓝色,B属于碱。写出B转化为A的化学方程式:________;A和E反应的化学方程式:________;B和E反应从微观角度分析其实质是________。
【答案】CO2+2NaOH=Na2CO3+H2O Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ 酸中的H+和碱中的OH-结合成H2O
【解析】
根据C是蓝色溶液可知,C为硫酸铜,B属于碱,则B为氢氧化钠;由于B(氢氧化钠)能与A相互转化,则A为碳酸钠,碳酸钠和氢氧化钙反应可以生成氢氧化钠,氢氧化钠和二氧化碳反应可以生成碳酸钠;而E即能与氢氧化钠反应,又能与碳酸钠反应,则E为硫酸,那么D则为氧化铜,氧化铜能和硫酸反应转化为硫酸铜;
根据分析知,B转化为A ,可以是二氧化碳和氢氧化钠的反应,方程式为:CO2+2NaOH=Na2CO3+H2O
A和E 的反应即碳酸钠和硫酸反应,方程式为: Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
B和E反应是酸和碱的反应,即中和反应,中和反应的实质是氢离子和氢氧根离子结合生成水。

【题目】活动小组为测定由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该固体混合物各20g,分别缓慢加入到50 g、100 g、150 g某稀硫酸中,测得三组实验数据如下表:
组别 | 第1组 | 第2组 | 第3组 |
稀硫酸质量/g | 50 | 100 | 150 |
剩余固体的质量/g | 10.0 | 4.0 | 4.0 |
根据实验及有关数据进行分析与计算:
(1)第1组实验中_____________(填“氧化铜”“稀硫酸”或“氧化铜与稀硫酸”)完全反应。
(2)样品中氧化铜的质量分数是__________g。
(3)根据第1组实验数据计算所用的稀硫酸溶质的质量分数__________(写出计算过程)。
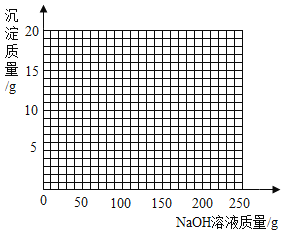
(4)若将第2组实验后的混合物过滤,在滤液中滴加10%的NaOH溶液,请画出在该混合溶液中加入10% NaOH溶液的质量与生成沉淀质量变化关系的曲线图__________。