题目内容
【题目】小萌将12.5g石灰石(主要成分是碳酸钙)投入盛有100g稀盐酸的烧杯中,恰好完全反应后,烧杯中剩余物的质量为108.1g试求:
(1)生成的CO2的质量为多少克?_______________
(2)12.5g石灰石中所含碳酸钙的质量是多少?_______________
(3)石灰石中所含碳酸钙的质量分数是多少?_______________
【答案】4.4g 10g 80%
【解析】
根据质量守恒定律,反应前后减少的质量为二氧化碳的质量,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳。
(1)生成的CO2的质量为![]()
(2)设参加反应的碳酸钙的质量为x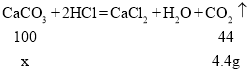
![]()
![]()
(3)石灰石中CaCO3的质量分数为![]()
答:生成二氧化碳的质量为4.4g;12.5g石灰石中所含碳酸钙的质量为10g;石灰石中CaCO3的质量分数为80%。

练习册系列答案
 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
【题目】在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的是:( )
物质 | M | N | Q | P |
反应前质量(g) | 18 | 1 | 2 | 32 |
反应后质量(g) | X | 26 | 2 | 12 |
A.该变化的基本反应类型是化合反应B.反应后物质M的质量为l3g
C.反应中N、P的质量比为5:3D.物质Q可能是该反应的催化
【题目】甲、乙、丙、丁四位同学分别进行了有关化学反应A+B=C的四组实验,各物质的质量如下表所示,已知四位同学取的A和B的总质量均为10g,且反应均完全进行。下列选项不正确的是
A/g | B/g | C/g | |
甲 | 7 | 3 | 9 |
乙 | 6 | 4 | 9 |
丙 | X | Y | 6 |
丁 | 5 | 5 | Z |
A.Y可能等于8B.X可能等于4
C.X可能等于8D.Z一定等于7.5