题目内容
为测定某石灰石样品中碳酸钙的质量分数,取22.2克石灰石样品,放入盛有146克稀盐酸的烧杯中,石灰石中的碳酸钙跟盐酸恰好完全反应(杂质既不反应也不溶解),烧杯内物质的质量变为159.4克.求:
(1)石灰石中碳酸钙的质量分数.
(2)稀盐酸中溶质的质量分数.
(3)生成物溶液中溶质的质量分数.
(1)石灰石中碳酸钙的质量分数.
(2)稀盐酸中溶质的质量分数.
(3)生成物溶液中溶质的质量分数.
分析:石灰石的质量与稀盐酸的质量和去掉烧杯内剩余物质的质量所得的质量是生成二氧化碳的质量.
由二氧化碳的质量根据碳酸钙与稀盐酸反应的化学方程式可以计算出石灰石中碳酸钙的质量、稀盐酸中溶质的质量分数和生成氯化钙的质量.进而计算出石灰石中碳酸钙的质量分数.
用石灰石的质量去掉碳酸钙的质量就是石灰石中杂质的质量,用烧杯内剩余物质的质量去掉石灰石中杂质的质量就是所得溶液的质量,氯化钙的质量与所得溶液的质量之比就是所得溶液中溶质的质量分数.
由二氧化碳的质量根据碳酸钙与稀盐酸反应的化学方程式可以计算出石灰石中碳酸钙的质量、稀盐酸中溶质的质量分数和生成氯化钙的质量.进而计算出石灰石中碳酸钙的质量分数.
用石灰石的质量去掉碳酸钙的质量就是石灰石中杂质的质量,用烧杯内剩余物质的质量去掉石灰石中杂质的质量就是所得溶液的质量,氯化钙的质量与所得溶液的质量之比就是所得溶液中溶质的质量分数.
解答:解:生成二氧化碳的质量为:146g+22.2g-159.4g=8.8g;
设石灰石中碳酸钙的质量为x,稀盐酸中溶质的质量分数为y,生成氯化钙的质量为z.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 111 44
x 146g×y z 8.8g
=
x=20g,
=
y=10%,
=
z=22.2g
石灰石中碳酸钙的质量分数为
×100%≈90.1%
所得溶液中溶质的质量分数为=
×100%≈14.1%
答:(1)石灰石中碳酸钙的质量分数为90.1%;
(2)盐酸溶液中溶质的质量分数为14.6%;
(3)反应后所得溶液中溶质的质量分数14.1%.
设石灰石中碳酸钙的质量为x,稀盐酸中溶质的质量分数为y,生成氯化钙的质量为z.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 111 44
x 146g×y z 8.8g
| 100 |
| x |
| 44 |
| 8.8g |
| 73 |
| 146g×y |
| 44 |
| 8.8g |
| 111 |
| z |
| 44 |
| 8.8g |
石灰石中碳酸钙的质量分数为
| 20g |
| 22.2g |
所得溶液中溶质的质量分数为=
| 22.2g |
| 159.4g-(22.2g-20g) |
答:(1)石灰石中碳酸钙的质量分数为90.1%;
(2)盐酸溶液中溶质的质量分数为14.6%;
(3)反应后所得溶液中溶质的质量分数14.1%.
点评:本题考查学生利用化学反应方程式的计算,明确二氧化碳是气体并利用质量守恒来计算二氧化碳的质量是解答的关键.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
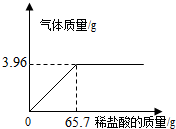 课题小组为测定某石灰石样品中CaCO3的含量,取l0g石灰石样品放在烧杯中,然后向其中注入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参与反应).随反应进行,注入稀盐酸的质量与反应得到气体的质量呈如图所示关系.请完成下列计算内容:
课题小组为测定某石灰石样品中CaCO3的含量,取l0g石灰石样品放在烧杯中,然后向其中注入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参与反应).随反应进行,注入稀盐酸的质量与反应得到气体的质量呈如图所示关系.请完成下列计算内容: