题目内容
【题目】实验室常用下图A、B或C装置制取气体,回答相关问题:
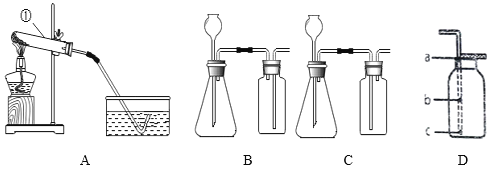
(1)图中①的仪器名称是___。
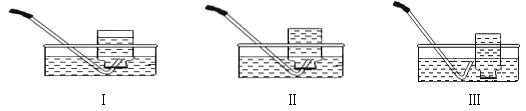
(2)小郭用A装置制取氧气,反应的符号表达式为___________________________________,为使整套装置处于完整的准备状态,下列将A装置中所缺仪器补画出来正确的是_______(填序号)。该实验中可能引起压强差导致试管炸裂的错误操作是________________________。
(3)用双氧水和二氧化锰来制取氧气时,可选用的装置是______(填“B”或“C”),另一装置若要完成实验在不变动导管的情况下如何操作_______________________________。
(4)利用装置D向上排空气法收集氧气,导管应伸到______(填“a”或“b”或“c”),验满氧气应该在_______(填“a”或“b”或“c”)。
(5)小强想用B装置制取氧气并控制反应速率,可将长颈漏斗换成_____________________。
【答案】 试管 KClO3![]() KCl + O2 Ⅲ 实验结束时,先熄灭酒精灯,再移导管 C 在集气瓶中装满水(或者集气瓶到放) c a 分液漏斗
KCl + O2 Ⅲ 实验结束时,先熄灭酒精灯,再移导管 C 在集气瓶中装满水(或者集气瓶到放) c a 分液漏斗
【解析】试题分析:本题主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了符号表达式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)图中①的仪器名称是试管;
(2)用A装置制取氧气,只能用氯酸钾与二氧化锰共热,生成氯化钾和氧气,其反应的符号表达式为KClO3![]() KCl + O2;A装置中缺少集气瓶,用排水法收集氧气时,集气瓶中应注满水,导气管应放于瓶口,所以选Ⅲ;实验结束时,若先熄灭酒精灯,再移导管,试管中气体温度下降,引起压强差,在气压的作用下水会倒流至试管中,引起试管的炸裂;
KCl + O2;A装置中缺少集气瓶,用排水法收集氧气时,集气瓶中应注满水,导气管应放于瓶口,所以选Ⅲ;实验结束时,若先熄灭酒精灯,再移导管,试管中气体温度下降,引起压强差,在气压的作用下水会倒流至试管中,引起试管的炸裂;
(3)用双氧水和二氧化锰来制取氧气时,可选用的装置是固液混合不加热型的装置,据此可选用B或C,又因为氧气的密度大于空气,只能选C,另一装置若要完成实验在不变动导管的情况下只要将集气瓶中装满水(或者集气瓶到放),即可完成实验;
(4)利用装置D向上排空气法收集氧气,导管应靠近集气瓶的底部,有利于空气的排出,所以选c,集气瓶口有氧气,才能称为集满,验满氧气时导管应该放在a处;
(5)分液漏斗可以控制液体的滴加速率,从而可控制反应的速率,所以小强用B装置制取氧气并控制反应速率,可将长颈漏斗换成分液漏斗。

【题目】某校兴趣小组在实验室中完成制取氧气的实验。他们取氯酸钾和二氧化锰的混合物共5.0 g放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
剩余固体质量/g | 4.55 | 3.75 | 3.30 | 3.08 | 3.08 |
分析表中数据,完成下列问题:
(1)完全反应后,生成氧气的质量为________g;
(2)原混合物中氯酸钾的质量分数是多少?(精确到0.1%)
【题目】课本“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性质实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁(Fe2O3)能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
实验步骤 | 实验现象 |
Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃, B试管中无明显现象 |
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag. | |
Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |
【实验结论】
(1)实验Ⅱ、Ⅲ证明:氧化铁的______和____________在反应前后均没有发生变化,可以作过氧化氢溶液分解的催化剂。
(2)写出氧化铁(Fe2O3)催化过氧化氢溶液分解的符号表达式_____________________。
【试验评价】实验设计Ⅳ的目的是比较_____________________。
【实验拓展】查阅资料得知:硫酸铜、马铃薯等也可以作过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是______________(填序号)。
A.MnO2是所有反应的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应速率
D.用作催化剂的物质也可能是其他反应的反应物或生成物