题目内容
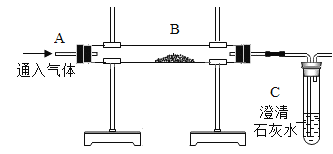
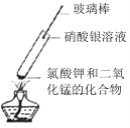
【题目】加热氯酸钾和二氧化锰的混合物可制备氧气:
该反应的化学方程式为_________, 但实验中发现有刺激性气味的气体产生。
[提出问题]刺激性气味的气体是什么呢?
[猜想假设]猜想一:臭氧(化学式为O3)
猜想二: HCl
猜想三: Cl2。
同学们认为不需要实验验证就可以判断猜想二是错误的,理由为____
[查阅资料]
(1) Cl2 +H2O=HClO + HCl,那么HC1O的相对分子质量为____
(2)臭氧在MnO2存在的情况下极易分解成氧气。
(3)氯气可使湿润的淀粉碘化钾试纸变蓝。
[实验探究]
查阅资料后大家认为猜想一是错误的,理由为____
[反思拓展]
(1)欲证明二氧化锰是氯酸钾分解的催化剂,需证明二氧化锰的____、______在反应前后不变。
(2)自来水厂常用氯气来杀菌消毒,氯气和水反应后会产生H+、Cl-和C1O-,而野外常用漂白粉主要成分化学式为Ca(C1O)2。你认为在水中起杀菌消毒作用的离子是____
【答案】2KClO3![]() 2KCl+3O2↑ 反应物中无氢元素 52.5 臭氧在MnO2存在的情况下极易分解成氧气 质量 化学性质 C1O-
2KCl+3O2↑ 反应物中无氢元素 52.5 臭氧在MnO2存在的情况下极易分解成氧气 质量 化学性质 C1O-
【解析】
加热氯酸钾和二氧化锰的混合物可制备氧气,原理是氯酸钾在二氧化锰的作用下受热分解生成氯化钾和氧气,该反应的化学方程式为2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
[猜想假设]不需要实验验证就可以判断猜想二是错误的,理由:据质量守恒定律可知反应前后元素的种类不变,反应物中无氢元素,不可能生成氯化氢;
[查阅资料]
HC1O的相对分子质量为:1+35.5+16=52.5;
[实验探究]
查阅资料后大家认为猜想一是错误的,理由为臭氧在MnO2存在的情况下极易分解成氧气;
[反思拓展]
(1)能改变其他物质的反应速率而本身的质量和化学性质在反应前后不变的物质叫催化剂。欲证明二氧化锰是氯酸钾分解的催化剂,需证明二氧化锰的质量、化学性质在反应前后不变;
(2)自来水厂常用氯气来杀菌消毒,氯气和水反应后会产生H+、Cl-和C1O-,而野外常用漂白粉主要成分化学式为Ca(C1O)2,溶液中离子为Ca2+和C1O-,相同的性质是由溶液中相同的微粒决定的,由此可知在水中起杀菌消毒作用的离子是C1O-。

 阅读快车系列答案
阅读快车系列答案