��Ŀ����
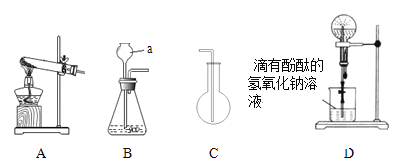
����Ŀ����һ��������̼��ط�ĩ���������ʿ���������ء�����ơ��Ȼ��ء��Ȼ�������̼�����е�һ�ֻ��֡�Ϊȷ����ɷ֣���������ʵ��:
(1)ȡ�����÷�ĩ���Թ��У���������ˮ����ܽ⣬�õ���ɫ������Һ�������Һ�м�����������������Һ���а�ɫ�����������ټ���������ϡ���ᣬ��ַ�Ӧ���ְ�ɫ������ʧ��
(2)��ȡ13.8g�÷�ĩ���ձ��У���ˮʹ����ȫ�ܽ⣬�ټ���200gһ�����������������Ȼ�����Һ��ǡ����ȫ��Ӧ������19.7g��ɫ������
(����:ϡ������̼�����ܷ������ֽⷴӦ��ϡ�������Ȼ�������Ӧ)
����˵����ȷ����
A. ������һ���������Ȼ�����
B. ������һ�������Ȼ��أ����ܺ�������ء�̼����
C. �ð���ĩ�����ֻ���������
D. �����Ȼ�����Һ�����ʵ���������Ϊ20.8%
���𰸡�AC
��������(1)ȡ�����÷�ĩ���Թ��У���������ˮ����ܽ⣬�õ���ɫ������Һ��˵�������Ȼ�������dz��ɫ��������ƣ�����ƻ���̼��ط�Ӧ����̼��Ƶij������������Һ�м�����������������Һ���а�ɫ�����������ټ���������ϡ���ᣬ��ַ�Ӧ���ְ�ɫ������ʧ���Ȼ�������������Ӧ���ɲ���ϡ���ᷴӦ�ij����Ȼ�����̼��������������Ӧ��������ϡ���ᷴӦ��̼�����ij�������˵����Һ�к����Ȼ��أ�̼������(2)
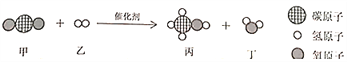
K2CO3+BaCl2=BaCO3��+2KCl Na2CO3+BaCl2=BaCO3��+2NaCl
138 197 106 197
13.8g 19.7g 10.6g 19.7g
������Ķ�Ӧ��ϵ��֪��������̼����13.8g���Ȼ�����Һ��Ӧ����19.7g��̼�ᱵ���������÷�ĩ�к����Ȼ��أ���̼���Ƶ�����С��13.8g����������̼��ء�̼�������������Ȼ�����Һ��Ӧ��̼��������̼�ᱵ�������ࡣ��ȡ13.8g�÷�ĩ���ձ��У���ˮʹ����ȫ�ܽ⣬�ټ���200gһ�����������������Ȼ�����Һ��ǡ����ȫ��Ӧ������19.7g��ɫ������˵����ĩ��һ������̼������A���ɷ�����֪��������һ���������Ȼ���������ȷ��B��������һ�������Ȼ�����̼���������ܺ����������������C���ð���ĩ����ɿ�����̼������Ȼ�����̼���Ƽ�̼��ء��Ȼ��ء�̼��������������������������ȷ��D���������Ȼ�����Һ�����ʵ�����Ϊx��
K2CO3+BaCl2=BaCO3��+2KCl
208 197
x 19.7g
![]()
x=20.8g
�����Ȼ�����Һ�����ʵ���������Ϊ![]() ��100��=10.4��������ѡAC��
��100��=10.4��������ѡAC��

 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�����Ŀ����ȤС��ͬѧΪ��̽��ʵ�����о��õ��������ɹ���ijɷ֣��������й�ʵ�顣
��1�����Թ�����룩
����һ��ȫ����NaOH���������ȫ����Na2CO3������������NaOH��Na2CO3�����
��2����ʵ����ƶϣ�Ϊ��һ��ȷ���ɷ֣�����������̽����
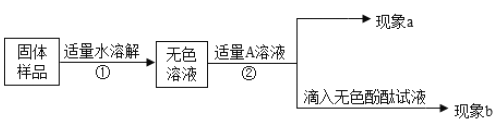
����ɫ��Һ��������ʵ�飺
ʵ����� | ʵ������ | ʵ����� |
��һ���� ���Թ�ȡԼ2mL����Һ��������������������Һ���� | ����a����ɫ���� | ��ѧ����ʽ�� ��____________________�� ��̼���Ʋ�ȫ�������� |
�ڶ����� ���ã�ȡ�ϲ���Һ���Թ��е����̪��Һ���� | ����b�� ��____________________ | ����NaOH����������������NaOH��Na2CO3����� |
��С������ͬѧ������ɣ���Ϊ����ʵ�鲻��֤�������������������ǣ�______��
�ܷ�˼���ѵ�һ���е�����������Һ����__________��Һ���ɴﵽʵ��Ŀ�ġ�
��3�������������ṩ���Լ����ṩ���Լ��У���̪��Һ��ϡ���ᡢ����������Һ���Ȼ�����Һ�������ʵ��֤������һ������������û�б��ʣ�����ȷ�ġ�����Ƶ�ʵ�鷽����__________________��