题目内容
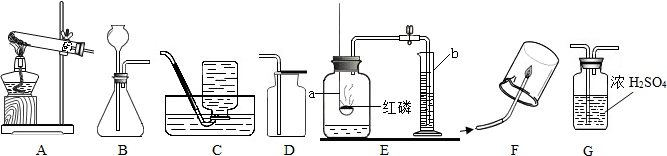
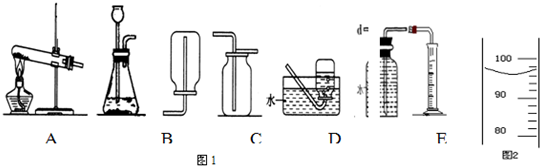
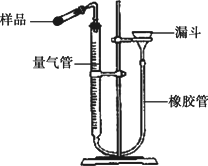
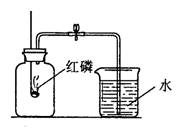
下图是实验室测定空气中氧气含量实验的装置图: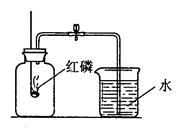
(1)红磷在空气中燃烧的文字表达式 ;
(2)实验时,燃烧匙里红磷要过量,其目的是 。
(3)该实验不仅可以说明氧气占空气的体积比,还可以得到氮气的两点性质是 , 。
(1)文字表达式 红磷+氧气 →五氧化二磷 ;
→五氧化二磷 ;
(2)目的 把氧气反应完(或耗尽氧气) ;
(3)物理性质 难溶于水 ;化学性质 不能燃烧,不能支持燃烧 。
解析

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目