题目内容
过氧化钙(CaO2)广泛应用于水产养殖、污水处理等领域,是优良的供养剂.
[制备CaO2]工业制备过氧化钙的一种方法是氢氧化钙法.
(1)Ca(OH)2和H2O2在有水存在的条件下生成CaO2·8H2O,它在120℃时完全分解为CaO2等.有关化学反应方程式为:________,________.
[测定CaO2纯度]CaO2在350℃时能迅速分解,生成CaO和O2.下图是实验室测定产品中CaO2含量的装置.
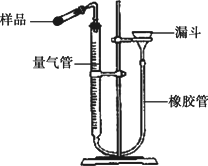
(2)检查装置气密性的方法是:连接好装置,从漏斗注水,量气管两边形成高度差,做好标记,一段时间后,高度差________,说明气密性良好.
(3)正确读取量气管内液面的初始、最终读数前都需进行的操作是________.
(4)加热小试管时,随着过氧化钙分解,量气管内的液面逐渐下降,为防止试管和量气管内气体压强过大,可将漏斗________(填“上提”或“下移”).
(5)计算含量需要测定的数据有________.(填字母序号)
A.氧气的体积
B.样品的质量
C.反应的时间
(6)若样品质量为0.20 g,反应前量气管读数为2.10 mL,反应后量气管读数为24.50 mL(常温下氧气的密度为1.429 g/L).实验中量气管的最佳规格是________.(填字母序号)
A.50 mL
B.100 mL
C.1 L
(7)样品中CaO2含量为________.
(8)若样品质量用w表示,反应前称量药品和小试管总质量为m g,反应后在空气中冷却,称量药品和小试管总质量为n g,则CaO2含量=![]() .此方案测定结果偏小的原因可能是________.
.此方案测定结果偏小的原因可能是________.
解析:
|
(1)Ca(OH)2+H2O2+6H2O=CaO2·8H2O CaO2·8H2O (2)不变 (3)调节两边液面相平 (4)下移 (5)AB (6)A (7)72% (8)在空气中冷却导致CaO吸收水蒸气 |

(6分)
长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙时产生气泡。
(1)提出问题:当把过氧化钙投入足量水中时,最终会生成什么物质呢?
(2)进行猜想:甲同学认为:生成氧化钙和氧气;
乙同学认为:生成氢氧化钙[Ca(OH)2]和氧气。
你认为 同学的猜想是错误的,其理由是 。
(3)设计实验:验证另一个同学的猜想是正确的,并填入下表空格中。
| 实验方法 | 实验现象 | 实验结论 |
| ①取少量过氧化钙放入试管中,加足量水,将带火星的木条伸进试管中。 |
| 有氧气生成 |
| ②取实验①静置后的上层清夜, 。 |
|
|

