题目内容
【题目】为测定某BaCl2溶液的溶质质量分数,现取100gBaCl2溶液,不断加入稀H2SO4,反应过程中溶液质量与加入稀H2SO4的质量关系如图所示,(反应方程式:BaCl2+H2SO4=BaSO4 ↓+2HCl)请回答:
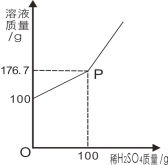
(1)P点意义_______________。
(2)反应生成BaSO4沉淀的质量为_________g。
(3)求原BaCl2溶液的溶质质量分数。
【答案】①完全反应 ②23.3③20.8%
【解析】
试题分析:刚开始会生成硫酸钡沉淀,所以溶液质量增加的较为缓慢,但当氯化钡完全反应后,溶液质量增加的救比较快,所以P点的含义是氯化钡和稀硫酸恰好完全反应,生成硫酸钡的质量为200-176.7=23.3g,求氯化钡溶液的溶质质量分数是根据化学方程式进行计算:设BaCl2质量为![]()
BaCl2 + H2SO4=BaSO4 ↓+ 2 HCl
208 233
![]() 23.3g
23.3g
![]() =
=![]()
![]()
![]()
原BaCl2溶液的溶质质量分数为![]() (1分)
(1分)

练习册系列答案
相关题目
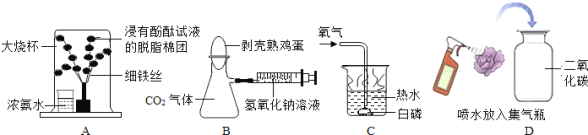
【题目】实验室有一瓶无色气体,可能是氧气或二氧化碳,完成下列问题。
操作 | 现象 | 结论 |
将_________________伸入集气瓶中 | ________________________ | 这瓶气体是氧气 |
向集气瓶中滴加适量________,振荡 | ________________________ | 这瓶气体是 二氧化碳 |