题目内容
【题目】中盐河南盐业配送中心构建现代化食盐流通体系,实行食盐专营,确保本地广大市民健康、安全的选购和食用食盐,同时为企业提供优质的化工原料。则回答问题:
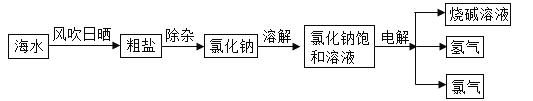
(1)精盐由粗盐提取,而粗盐主要成分为NaCl,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。
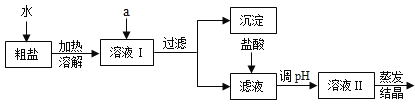
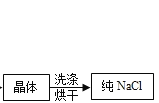
(提供的试剂):Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
①欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、________、________;
②在滤液中加盐酸的作用是_____________;
(2)用提纯的NaCl配制200g溶质质量分数为0.9%的生理盐水,需要NaCl的质量为_______g。
①配制该溶液时所需要的玻璃仪器有________________;
②如果配制后溶液溶质的质量分数低于0.9%,你认为可能的原因是________(一点即可)。
【答案】BaCl2溶液 Na2CO3溶液 除去过量的NaOH和Na2CO3 1.8 烧杯、玻璃棒、量筒、胶头滴管 称量NaCl的操作错误,如左盘放了纸片,右盘未放纸片(或用量筒量水时仰视读数,烧杯中有水,氯化钠中混有杂质等)
【解析】
(1)①根据除去溶液I中的MgCl2、CaCl2、Na2SO4,需要用氢氧化钠除去氯化镁,用氯化钡除区硫酸钠,用碳酸钠除去氯化钙与多余的氯化钡进行分析;
②根据在除杂过程中加入的氢氧化钠、碳酸钠是过量的,仍是杂质,盐酸会与氢氧化钠反应生成氯化钠和水,与碳酸钠反应生成氯化钠水和二氧化碳进行分析;
(2)根据溶质质量分数的计算公式和配制溶液的方法和所用仪器,以及配制后溶液溶质的质量分数低于0.9%,要从造成溶质质量少或溶剂质量多的原因进行分析。
(1)①要除去溶液I中的MgCl2、CaCl2、Na2SO4,所选试剂分别是氢氧化钠溶液,碳酸钠溶液和氯化钡溶液,依据题意要求,为了更好的把杂质除去,不带入新的杂质,所加溶液的顺序是氢氧化钠溶液,过量的BaCl2溶液,过量的Na2CO3溶液;
②由于过滤后的滤液中含有氢氧化钠和碳酸钠,所以要加入适量的盐酸,目的是除去过量的NaOH和Na2CO3;
(2)氯化钠溶质的质量等于溶液的质量×溶质的质量分数,即200g×0.9%=1.8g;
①配制溶液需要的玻璃仪器有:烧杯、玻璃棒、量筒、胶头滴管;
②称量NaCl的操作错误,如左盘放了纸片,右盘未放纸片;用量筒量水时仰视读数;烧杯中有水;氯化钠中混有杂质等都可能导致配制后溶液溶质的质量分数低于0.9%。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案