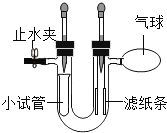
题目内容
【题目】工业上制造高纯度 CaO 的主要流程示意图如下:
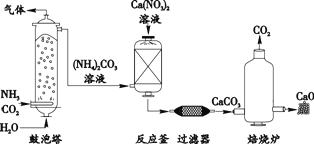
(1)CaCO3 中碳元素的化合价是_________。
(2)反应釜中发生的反应属于复分解反应,其化学方程式是________。
(3)焙烧炉中,CaCO3 在 1000 ℃可分解得到高纯度 CaO。理论上 5 t CaCO3 制出CaO 的质量是________ t。稍冷后,取出 CaO 立即放入干燥器,其原因是________(用化学方程式表示)。
【答案】+4 Ca(NO3)2 + (NH4)2CO3 =2NH4NO3 + CaCO3↓ 2.8 CaO + H2O ===Ca(OH)2
【解析】
解:(1)在CaCO3中,设碳的化合价为x,(+2)+x+(-2×3)=0,解得:x=+4;
(2)反应釜中硝酸钙与碳酸铵反应生成硝酸铵和碳酸钙,属于复分解反应,其化学方程式是Ca(NO3)2+(NH4)2CO3═2NH4NO3+CaCO3↓;
(3)设制出CaO 的质量是x,
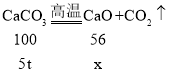
![]()
x=2.8t;
冷后,取出 CaO 立即放入干燥器,防止氧化钙与空气中的水蒸气反应生成氢氧化钙,化学方程式为:CaO+H2O═Ca(OH)2。

练习册系列答案
相关题目