题目内容
【题目】请结合图回答问题:
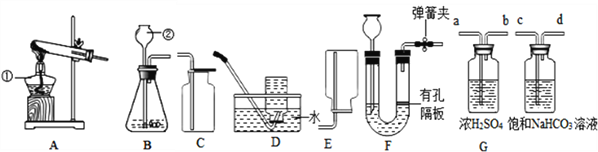
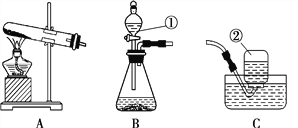
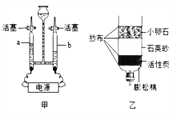
(1)标号①②的仪器名称:①:______________,②:________________.
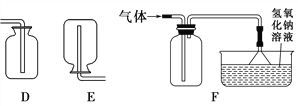
(2)实验室选用B、D装置制取O2并做铁丝在其中燃烧实验,当集气瓶中水__________时停止收集。(填“全部排出”或“大部分排出”).
(3)选择_________装置组合(选填序号)可以用于实验室制取干燥的O2或CO2,若将发生装置改为F制CO2,其优点是:________________________.
(4)用化学反应方程式表示在制取纯净的CO2的过程中饱和碳酸氢钠溶液的作用:_____.
【答案】 酒精灯 长颈漏斗 大部分排出 BGC 便于控制反应的发生与停止 NaHCO3 + HCl =NaCl + H2O + CO2↑
【解析】本题主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的除杂等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)标号①②的仪器名称分别是酒精灯、长颈漏斗;
(2)在做铁丝在氧气燃烧实验时,为了防止燃烧产生的固体溅落瓶底引起集气瓶的炸裂,需在集气瓶底部放少量的水。实验室选用B、D装置制取O2并做铁丝在其中燃烧实验,集气瓶中的水大部分排出时停止收集;
(3)根据题意用同一装置制取O2、CO2,应用固体和液体混合制取氧气,发生装置选B,二氧化碳、氧气的密度比空气大,可用向上排空气法来收集,收集装置选G,干燥二氧化碳、氧气应用浓硫酸,干燥装置选用C,所以选择BGC装置组合可以用于实验室制取干燥的O2或CO2,发生装置F通过弹簧夹的开或关,在大气压强的作用下,能将固体和液体接触或分离,能控制反应的发生与停止。若将发生装置改为F制CO2,其优点是便于控制反应的发生与停止;
(4) 盐酸具有挥发性,用大理石与盐酸反应制得的二氧化碳的气体中有少量的氯化氢气体,氯化氢溶于水形成盐酸,碳酸氢钠溶液与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式是NaHCO3 + HCl =NaCl + H2O + CO2↑。

【题目】镁条在空气中久置表面会变黑,某小组同学设计进行实验,探究镁条变黑的条件。
(查阅资料)常温下,亚硫酸钠(Na2SO3)可与 O2 发生化合反应。
(猜想与假设)常温下,镁条变黑可能与 O2、CO2、水蒸气有关
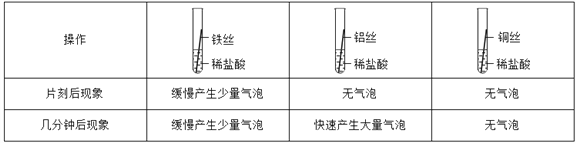
(进行实验)通过控制与镁条接触的物质,利用下图装置(镁条长度为 3cm,试管容积为20mL),分别进行下列 5 个实验,并持续观察 20 天。
编号 | 主要实验操作 | 实验现象 |
1 | 先充满用 NaOH 浓溶液洗涤过的空气再加入 2mL 浓硫酸 | 镁条始终无明显变化 |
2 | 加入 2mL NaOH 浓溶液 | 镁条始终无明显变化 |
3 | 先加入 2mL 浓硫酸再通入约 4mL CO2 | 镁条始终无明显变化 |
4 | 先加入 4mL 饱和 Na2SO3 溶液再充满 CO2 | 镁条始终无明显变化 |
5 | 先加入 2mL 蒸馏水再通入约 4mL CO2 | 镁条第 3 天开始变黑至第 20 天全部变黑 |
(解释与结论)
(1)实验1 和 2 中,NaOH 浓溶液的作用是_____(用化学方程式表示);
(2)实验1 的目的是_____;
(3)实验3 中,试管内的气体主要含有 CO2、_____;
(4)得出“镁条变黑一定与CO2 有关”结论,依据的两个实验是_____(填编号);
(5)由上述实验可推知,镁条变黑的条件是_____;
(反思与评价)
(6)在猜想与假设时,同学们认为镁条变黑与 N2 无关,其理由是_____;
(7)本 组 实 验 1/2 中 使 用 的 NaOH 浓 溶 液 , 而 不 是 使 用 澄 清 石 灰 水 , 理 由 是_____。