题目内容
【题目】科学兴趣小组做了如下实验:将一镁条放入CuCl2溶液中,镁条表面覆盖了红色物质,但很快镁条表面又冒出很多气泡,他们觉得很奇怪. 
(1)【提出问题】这些气泡究竟是怎样产生的?是什么气体呢? 【猜想】小科:是氧气;小丽:是氯化氢;小琪:是氨气(NH3);小梁:是氢气.小黄马上否定了小琪的猜想,他否定的依据是;
(2)【实验探究】他们开始着手收集所产生的气体. 实验一:小科用带火星的木条检验该气体,木条不复燃.说明生成的气体不是氧气;
实验二:为继续探究反应后生成的气体是否是氯化氢,小丽用湿润的蓝色石蕊试纸检验该气体,试纸不变红,说明生成的气体不是氯化氢;
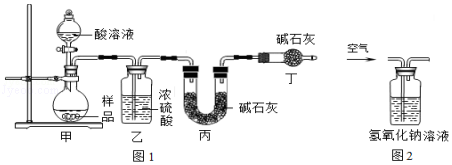
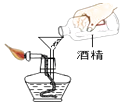
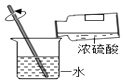
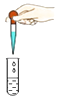
实验三:为确定气体是否是氢气,小梁设计了如图的实验装置(每个装置的反应均完全).
【实验结论】
(1 )若该气体是氢气,则在乙装置中可以观察到的现象是 .
(2 )甲、丙装置中无水硫酸铜的作用是不同的,请指出它们的区别 .
(3 )为确定该气体产生的本质原因,小梁用精密pH试纸测试实验所用的CuCl2溶液,pH约为5.5,最后确定CuCl2溶液呈酸性.查阅资料发现:CuCl2为强酸弱碱盐,其水溶液酸碱性与实验结果相符.
【答案】
(1)质量守恒定律(或反应物中没有氮元素)
(2)黑色粉末变红;甲是除去原气体中的水蒸气,丙是验证有水生成
【解析】解:【猜想】反应物是镁和CuCl2溶液,没有N元素,根据质量守恒定律可知,小琪的猜想不对;【实验结论】(1)氢气具有还原性,能够还原氧化铜,生成红色铜.所以若该气体是氢气,则在乙装置中可以观察到的现象是黑色粉末变红;(2)检验气体的成分,首先除去水分的干扰,无水硫酸铜能够吸收水分,所以甲中的无水硫酸铜是除去原气体中的水蒸气;无水硫酸铜遇水变蓝,所以无水硫酸铜可以检验水分的存在,丙中的无水硫酸铜是验证有水生成. 所以答案是:【猜想】质量守恒定律(或反应物中没有氮元素);
【实验结论】(1)黑色粉末变红;(2)甲是除去原气体中的水蒸气,丙是验证有水生成.
【考点精析】关于本题考查的质量守恒定律及其应用,需要了解①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏才能得出正确答案.