题目内容
【题目】分离与提纯是获得物质的重要方法。下列实验操作能达到实验目的的是
实验目的 | 实验操作 | |
A | 除去二氧化碳气体中的一氧化碳 | 通入适量氧气,点燃 |
B | 除去氯化钠固体中的泥沙 | 加入足量的水溶解,过滤,蒸发结晶 |
C | 除去氯化钙溶液中的盐酸 | 加入过量的碳酸钙固体,充分反应后过滤 |
D | 除去碳酸钠溶液中的氯化钠 | 加入过量的硝酸银溶液,过滤 |
A.AB.BC.CD.D
【答案】BC
【解析】
A、二氧化碳不燃烧,也不支持燃烧,二氧化碳中混有少量一氧化碳,无法点燃,不符合题意;
B、氯化钠溶于水,泥沙不溶于水,加入足量的水,溶解、过滤,除去泥沙,蒸发结晶可得氯化钠固体,符合题意;
C、碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水,充分反应后,过滤,除去过量的碳酸钙,可得氯化钙溶液,符合题意;
D、加入过量的硝酸银,硝酸银和氯化钠反应生成氯化银和硝酸钠,碳酸钠与硝酸银反应生成碳酸银和硝酸钠,虽然除去了杂质,也除去了原物质,且引入了新的杂质硝酸银和硝酸钠,不符合题意。
故选BC。

【题目】(2017云南)小明同学在课外阅读中得知:钠是一种活泼金属,常温下能与氧气、水发生反应,其中钠与水反应的化学方程式为:2Na+2H2O= 2NaOH+H2↑。在实验室,该同学先取50 mL一定溶质质量分数的硫酸铜溶液于烧杯中,再取绿豆大小的钠投入硫酸铜溶液中,充分反应后过滤,得到滤液和蓝色滤渣,并对滤液的成分进行探究。
(提出问题)滤液中的溶质的成分是什么?
(查阅资料)已知Na2SO4的水溶液呈中性。
(猜想与假设)猜想一:Na2SO4;
猜想二:_________;
猜想三:Na2SO4、CuSO4;
猜想四:Na2SO4、CuSO4、NaOH。
其中猜想不合理的是________。
(实验方案与验证)
实验 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量滤液于试管中,观察现象 | 溶液为无色 | 猜想____不成立 |
实验二 | 另取少量滤液于试管中,向其中滴加酚酞试剂 | 无明显现象 | 猜想____不成立 |
实验三 | 常温下,再取少量滤液,测溶液酸碱度 | pH=7 | 猜想____成立 |
(拓展延伸)金属钠在运输、保存中应该注意:___________。
【题目】(10分)某校化学兴趣小组就空气中氧气的含量进行了分组实验探究。
Ⅰ组:(1)Ⅰ组同学讨论后认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应而且生成物为固体。他们应该选择_________(填序号),为了充分消耗容器中的氧气,药品的用量应保证_______________________。
A.蜡烛 B.红磷 C.铁丝 D.木炭
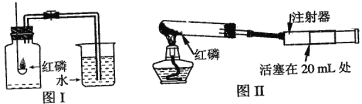
(2)小组同学共同设计下图所示的两套装置,你认为合理的是______(填序号)。为了确保实验的成功,在装药品之前应该
____________________________________________。
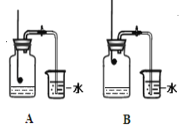
(3)在讨论的基础上,他们分组进行了实验。
【数据分析】实验结束后,整理数据如下:(注:集气瓶容积为100 mL)
组别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入集气瓶中水的体积/mL | 20 | 21 | 19 | 20 | 22 | 19 |
(4)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的_________。
Ⅱ组:Ⅱ组同学发现Ⅰ组实验可能产生实验误差,对实验进行了改进,下图是Ⅱ组同学测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题。
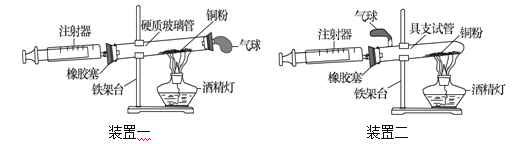
(1)根据下表提供的实验数据,完成下表
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
15mL | 15mL | 9mL |
(2)装置中气球的作用是 。
(3) 装置一和装置二中气球的位置不同, (填“装置一”或“装置二”)更合理,理由是 。
(4) 如何检查该装置的气密性? 。