题目内容
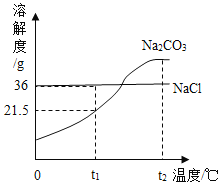
【题目】溶解度曲线的意义与应用可从点、线、面和交点四方面来分析。如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )

A.t2℃时,将a、b、c三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量大小关系是b>a=c
B.t2℃时,将50g a物质(不含结晶水)放入100g水中充分溶解得到a的饱和溶液
C.将c的饱和溶液变为不饱和溶液,可采用降温的方法
D.t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c
【答案】A
【解析】
A、t1℃时,b物质的溶解度最大,a物质次之,a、b物质的溶解度随温度的降低而减小,会析出晶体,c物质的降低温度,不会析出晶体,应该按照t2℃时进行计算,所以将t2℃时,a、b、c三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是b>a>c,故错误,符合题意;
B、t2℃时,a的溶解度是50克。即t2℃时,在100克水中,最多能溶解50克a就能形成饱和溶液,故正确,不符合题意;
C、c物质的溶解度随温度的升高而减小,所以将c的饱和溶液变为不饱和溶液,可采用降温的方法,故正确,不符合题意;
D、根据三种物质的溶解度曲线不难看出,在t2℃时,a、b、c三种物质的溶解度大小关系为:a>b>c,故正确,不符合题意。
故选:A。

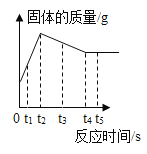
【题目】某化学兴趣小组使用如图所示装置,对某种铁铜合金的成分进行测量,先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品开始计时,并将电子天平的读数记录在下表中,请回答下列问题:

空烧杯 | 加入 硫酸后 | 加入铁粉后 5分钟 | 加入铁粉后 12分钟 | 加入铁粉后 21分钟 | 加入铁粉后 40分钟 | 加入铁粉后 3小时 | |
读数(g) | 28.5 | 169.7 | 183.6 | 183.5 | 183.4 | 183.3 | 183.3 |
(1)完全反应后,生成氢气的总质量为_________。
(2)合金中铁元素的质量分数为多少? __________
【题目】某化学兴趣小组同学,用盐酸和氢氧化钠进行“酸碱中和反应”的探究,进行一段时间后发现没有明显变化,询问老师才知道忘记滴加指示剂。因此,他们停止实验,并在老师的指导下对烧杯内的溶液中的溶质的成分进行探究。
(提出问题)该烧杯内的溶质是什么?
(猜想假设)猜想一:NaCl 猜想二:NaCl和HCl
猜想三:NaCl和NaOH 猜想四:NaCl、NaOH和HCl
同学们讨论后一致认为猜想四不合理,请你说出不合理的理由_____
(查阅资料)NaCl溶液呈中性。
(实验探究)兴趣小组甲、乙、丙三位同学分别设计了如下的实验方案,请你帮助他们完成实验报告的相关内容。
实验方案 | 实验现象 | 实验结论 |
甲同学取少量烧杯内的溶液于试管中,滴入酚酞试液 | 溶液无变化 | 猜想一成立 |
乙同学另取少量烧杯内的溶液于试管中,加入_____。 | 有气泡生成 | 猜想二成立 |
丙同学另取少量烧杯内的溶液于试管中,滴加适量的CuSO4溶液 | 没有蓝色沉淀产生 | 猜想_____不成立 |
(评价反思)老师看了甲、乙、丙三位同学的实验报告,指出甲同学的实验结论不准确,请你分析甲同学实验结论不准确的原因:_____。
(得出结论)猜想二成立
(拓展延伸)某同学在进行酸碱中和滴定实验时,测得溶液的pH变化如下图1所示,请回答下列问题:
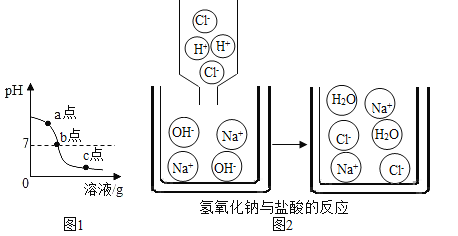
(1)由图1可知,该同学实验操作是_____。
A 将盐酸滴入氢氧化钠溶液中
B 将氢氧化钠溶液滴入盐酸中
(2)由图1可知,在b点处溶液中溶质是_____。
(3)图2为盐酸和氢氧化钠溶液反应的微观过程,从微粒的角度分析,此反应的微观实质 _____(合理答案即可)。
【题目】对比实验是化学研究中经常采用的方法。化学兴趣小组的同学在研究CO2通入NaOH溶液是否发生了反应,设计了下列二组实验。请和化学兴趣小组的同学一起探究并回答问题:
(设计与实验)
实验 序号 | 实验步骤一 | 实验步骤二 | 实验 序号 | 实验步骤一 | 实验步骤二 |
实验I |
|
| 实验II |
|
|
(探究与结论)
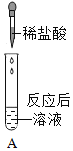
(1)实验I中步骤一看不到明显现象,步骤二产生的现象是______。
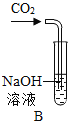
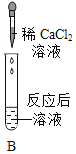
(2)实验Ⅱ中步骤二看到有白色沉淀析出,则发生反应的化学方程式是______。
(3)在实验Ⅱ的步骤一中CO2和NaOH溶液一定发生了化学反应,但却看不到明显的现象,原因是______。
(拓展延伸)现有下列信息:

请你和化学兴趣小组的同学一起利用以上资料信息再设计实验Ⅲ,证明CO2确实与NaOH发生了化学反应。
实验Ⅲ的操作为:______。
看到的现象是______。