题目内容
6.图为实验室制取二氧化碳及其性质的探究: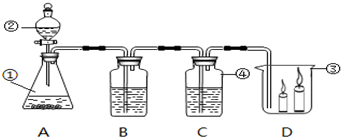
(1)写出图中标号仪器的名称:①锥形瓶;②分液漏斗;③烧杯
(2)实验开始前,应先检查装置A的气密性.
(3)实验室用装置A来制取CO2所用的药品是大理石;稀盐酸(填名称).
(4)若要用装置B鉴定CO2,连接AB,B中应盛放的试剂名称是澄清的石灰水,B中的实验现象是澄清的石灰水变浑浊,反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.
(5)收集二氧化碳用向上排空气法(填“向上排空气法”、“向下排空气法”或“排水法”),不用其他方法的原因是密度比空气大,能溶于水.
(6)怎样检验集气瓶中的二氧化碳气体己收集满?将带燃着的木条放在集气瓶口,若熄灭证明已满.
(7)若用装置C证明CO2能与水反应生成碳酸,连接AC,C中除有少量水外,还应加入的试剂是紫色石蕊试液装置C中观察到的现象是紫色石蕊试液变红,反应的化学方程式为CO2+H20=H2CO3.
(8)装置D中放有燃着的蜡烛如上图所示,连接AD,D中观察到的现象是下层的蜡烛先熄灭,上层的蜡烛后熄灭,说明二氧化碳的性质有不燃烧,也不支持燃烧;密度大于空气,二氧化碳在生活中可用于灭火.
分析 (1)根据装置图中仪器图,写出仪器的名称即可.
(2)制取气体的装置都要检查装置的气密性.
(3)根据实验室制取二氧化碳的药品进行分析解答.
(4)根据二氧化碳气体的检验方法进行分析解答.
(5)根据二氧化碳的化学性质进行分析解答.
(6)根据二氧化碳的验满方法进行分析解答.
(7)用装置C证明CO2与水反应生成碳酸,装置C中除水外还应加入的试剂是紫色石蕊试液,紫色石蕊试液变红,说明二氧化碳与水反应生成了碳酸;
(8)根据二氧化碳的性质(不能燃烧,不能支持燃烧,密度比空气大)进行分析解答.
解答 解:(1)图中标号仪器的名称:①为锥形瓶;②为分液漏斗;③为烧杯.
(2)制取二氧化碳前,要检验装置的气密性,不漏气才能进行实验.
(3)实验室常用大理石(或石灰石,其主要成分都是碳酸钙)和稀盐酸反应来制取二氧化碳.
(4)检验二氧化碳要用澄清的石灰水,若澄清的石灰水变浑浊,证明该气体是二氧化碳.二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
(5)收集二氧化碳用向上排空气法,不用其他方法的原因是 密度比空气大,能溶于水.
(6)检验集气瓶中的二氧化碳气体己收集满的方法为:将带燃着的木条放在集气瓶口,若熄灭证明已满.
(7)若用装置C证明CO2能与水反应生成碳酸,连接AC,C中除有少量水外,还应加入的试剂是紫色石蕊试液,紫色石蕊试液变红,说明二氧化碳与水反应生成了碳酸;故答案为:紫色石蕊试液;紫色石蕊试液变红;H2O+CO2=H2CO3
(8)烧杯中放有燃着的高低不同的蜡烛,实验现象是:蜡烛火焰由下而上依次熄灭,说明CO2具有不燃烧,也不支持燃烧、密度大于空气的性质,生活中常用于灭火;故答案为:蜡烛火焰由下而上依次熄灭;不燃烧,也不支持燃烧;密度大于空气;灭火;
故答案为:
(1)长颈漏斗;烧杯;(2)气密性;(3)大理石;稀盐酸;(4)澄清的石灰水; 澄清的石灰水变浑浊,Ca(OH)2+CO2═CaCO3↓+H2O.
(5)向上排空气法,密度比空气大,能溶于水.(6)将带燃着的木条放在集气瓶口,若熄灭证明已满.
(7)紫色石蕊试液,紫色石蕊试液变红,CO2+H20=H2CO3.
(8)下层的蜡烛先熄灭,上层的蜡烛后熄灭,不燃烧,也不支持燃烧;密度大于空气,灭火.
点评 本题难度不大,掌握二氧化碳的实验室制法的反应原理、二氧化碳的化学性质是正确解答本题的关键.注意不同的装置,检查气密性的方法不同,例如检查A装置气密性的方法是:将装置中导气管上的胶皮管用弹簧夹夹住,向分液漏斗中注水至形成一段液柱,一段时间后若液柱不下降,即可证明装置不漏气.

| A. | 在表面刷一层油漆 | B. | 在表面涂上机油 | ||
| C. | 在表面镀上一层其它金属 | D. | 使其表面生成致密氧化膜 |
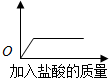
| A. | 生成氯化钠的质量 | B. | 溶液温度变化 | ||
| C. | 溶液中水的质量 | D. | 溶液中氯化氢的质量 |
| A. | 铁丝燃烧生成固体的质量比铁丝的质量大 | |
| B. | 物质升华时要吸收热量 | |
| C. | 36g水完全电解生成4g氢气和32g氧气 | |
| D. | 5g糖放入25g水中得到30g糖水 |
| A. | 加热铜丝时,红色固体会变成黑色 | |
| B. | 木炭在氧气中燃烧,生成黑色固体 | |
| C. | 加热“铜绿“时,绿色固体会变成黑色 | |
| D. | 铁丝在空气中燃烧时,火星四射,生成黑色固体 |
| A. | 蔗糖溶于水 | B. | 冰糖研碎 | C. | 生石灰溶于水 | D. | 海水晒盐 |
| A. | 试管内壁有油脂时,可用热的纯碱溶液洗涤 | |
| B. | 在粗盐提纯实验中,将滤液蒸干后停止加热 | |
| C. | 向试管中滴加液体时,滴管应紧贴试管内壁 | |
| D. | 过滤时,滤液高于滤纸边缘 |