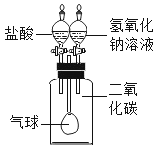
题目内容
【题目】如图是A、B固体物质的溶解度曲线
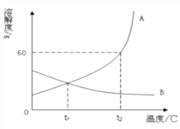
(1)将t2℃时160g A物质的饱和溶液蒸干, 理论上可以得到A物质的质量是________g。
(2)将t2℃两种物质的饱和溶液 降温到t1℃,溶液中溶质的质量分数是A______B。 (填“﹥”“﹤”“=”)
(3)若A物质中混有少量的B物质,可以用______方法提纯A.
(4)现有B物质的不饱和溶液,可以用_______的方法使之变为饱和溶液(填“升高温度”或“降低温度”).B物质有可能是______(用化学式表示)。
(5)“冬天捞碱,夏天晒盐”,句中的“碱”的溶解度曲线符合图中的_______物质的溶解度曲线。
【答案】 60 ﹥ 降温结晶 升高温度 Ca(OH)2 A
【解析】根据所学知识和题中信息知,(1)t2℃时A物质的溶解度是60g,160g A物质的饱和溶液蒸干, 理论上可以得到A物质的质量是160g﹣100g=60g。(2)A物质溶解度随温度升高而增大,B物质溶解度随温度升高而减少,t1℃时两者溶解度相等,t2℃时A溶解度大于B,将t2℃两种物质的饱和溶液降温到t1℃,溶液中溶质的质量分数是A﹥B。(3)若A物质中混有少量的B物质,可以用降温结晶方法提纯A。(4)现有B物质的不饱和溶液,可以用升高温度的方法使之变为饱和溶液,B物质有可能是Ca(OH)2,Ca(OH)2 溶解度随温度升高而减少。(5)“冬天捞碱,夏天晒盐”,句中的“碱”的溶解度曲线符合图中的A物质的溶解度曲线。
点睛∶Ca(OH)2 溶解度随温度升高而减少。

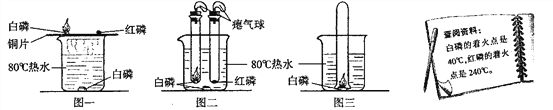
【题目】某些铜制品在空气中久置,表面生成绿色的铜锈(又称铜绿)。某化学实验小组设计并进行实验,探究铜锈的组成和铜生锈的条件。
I.探究铜锈的组成
【查阅资料】① 铜锈受热易分解 ② 硫酸铜粉末遇水由白色变为蓝色
【进行实验】 小组同学从铜器上取下适量的干燥铜锈,按图所示装置实验(部分夹持装置已略去)。观察到B中白色粉末变为蓝色,C中澄清石灰水变浑浊。
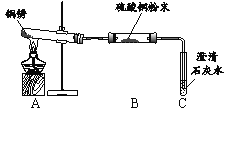
【解释与结论】(1)C中反应的化学方程式是______。
(2)依据以上现象分析,铜锈中一定含有的元素:Cu和______。
II.探究铜生锈的条件
【提出猜想】根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
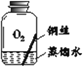
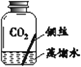
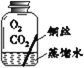
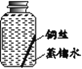
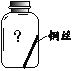
【进行实验】实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
现象 | 无明显现象 | 无明显现象 | 铜丝表面 有绿色物质 | 无明显现象 | 无明显现象 |
【解释与结论】
(3)实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是______。
(4)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是______(填编号)。
(5)对比实验②和③,得出的结论是______。
(6)为验证猜想,请在图中将实验⑤补充完整。______
(7)由上述实验可推知,铜生锈的条件是______。
【反思与应用】
(8)结合上述实验,你对保存铜制品的建议是______。
【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
A | B |
|
|
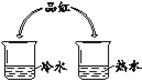
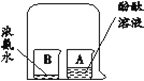
从微粒角度解释: (1)品红在水中扩散的原因是______。 (2)品红在热水中扩散速度快,其原因是______。 | (1)实验现象是______。 (2)实验结论是______。 |