��Ŀ����
������������õ����յȹ�Ч�����������ϲ����������ʾ�������к�̼���80��93%��������4��14%��ˮ��2��4%��ʮ���ְ����ᡢ28����Ԫ�ء�Ȼ��һЩ���������û��յı��Ǽ��Ϲ�ҵ�������������Ƶ�ҩˮ������ϴ����ɹ�Ժ�ֱ�Ӽӹ����ۣ�����Ҫ�ɷ��ǣ�̼��ƣ������������������ơ�������ij��ѧ��ȤС����Ʊ��������飬���ⶨ������̼��ƺ�����ʵ��̽��������
��̽��һ�����������������١�
����ֱ�����ˮ����ֽ��衢���ã��ⶨ�ϲ���Һ��pH����pH 7���>����<����=����Ϊ�����飬������ ��
��̽�������ⶨ������̼��ƺ�����
С����ͼ��ʾװ�òⶨ���������̼��Ƶĺ�����ʵ�鷽�����£�
�ż��װ�������ԣ���ͼ����װ���ú�ע���������������ǻ�����Ħ�������أ���ͬ���ӿ̶�1mL�����������̶�20mL���� (����������������������ã�
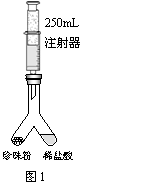
����ͼ����װ�������װ��1.1g �����������Ʒ���ҹ��ڵ���һ������ϡ���ᣬע���������Ϊ250mL�������Ƶ��ײ����ٴ�����װ�ã�
���跨ʹ���������ڵ�ҩƷ��ϣ���Ӧ�������ȡע��������Ϊ220mL��
�����ݴ���������ø��������̼��Ƶ���������Ϊ ���ۦѡ�CO2��=2g/L���������С�����1λ��
��ʵ��˼����
�Ŵ�ʵ���еķ�Ӧԭ���� (�û�ѧ����ʽ��ʾ)��
�ƿ���ע�������أ���ʵ�鷽��������۵����������Ƿ������Ҫ�� ��
�ǡ�̽�������еĵڢDz����������ҩƷ�ķ����� ��
�ȸ�ʵ��װ������ϵ��ŵ����� ��д��1�㼴�ɣ���
��̽��һ��> ��1�֣� �������в�����������ʹ����Һ�ʼ��ԣ�1�֣�
��̽���������ɿ�ע�����������������»ص�1mL�̶ȴ���2�֣��� 90.9%��2�֣�
��ʵ�鷴˼����CaCO3 + 2HCl = CaCl2 + H2O + CO2����1�֣�
����Ҫ�������������̫������CO2������������ע�����������ƣ�������������1�֣�
�ǽ�����װ��������б��ʹϡ����������߹��ڡ���1�֣�
�ȷ�������Ͳ����������������ֹ��������ۻ��ʱ���ֳ�������ȣ���1�֣�
���������������̽��һ���������⣬���������Ҫ�ɷ��ǣ�̼��ƣ������������������ƣ��ʽ�������ˮ����ֽ��衢���ã������ϲ���ҺӦ�Լ��ԣ���pH>7��
��̽����������װ�����������ã���ע���������ӿ̶�1mL�����������̶�20mL��ʱ��װ���ڵ�ѹǿ���С�����ɿ�ע�����������ڴ���ѹ�������£��������»ص�1mL�̶ȴ���
�ȸ������⣬��Ӧ�������ȡע��������Ϊ220mL����˵����Ӧ���ɶ�����̼����Ϊ220mL���������̼������=0.22L��2g/L=0.44g��
����������̼��Ƶ�����Ϊx
CaCO3 + 2HCl = CaCl2 + H2O + CO2��
100 44
x 0.44g
100:44=x:0.44g
���x=1g
����������̼��Ƶ���������=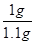 ��100%=90.9%
��100%=90.9%
��ʵ�鷴˼����̼��ƺ����ᷴӦ�������Ȼ��ơ�ˮ�Ͷ�����̼���ʷ�Ӧ�Ļ�ѧ����ʽΪCaCO3 + 2HCl = CaCl2 + H2O + CO2����
�������������̫��������CO2���������ᳬ��ע�����������ƣ������������ʸ�ʵ�鷽����Ҫ��������۵�������
�ǽ�����װ��������б��ʹϡ����������߹��ڡ�
�ȸ�ʵ��װ�ò������㣬���ڷ�Ӧʼ�����ܱ�װ������ɣ��ʲ�������������ȷ��ͬʱ���ڻ��������ɻ���ܷ�ֹ��������ۻ��ʱ���ֳ�������
���㣺ʵ��̽�����ʵ���ɳɷ��Լ����������װ�õ������ԣ���Ļ�ѧ���ʣ�̼���ơ�̼��������̼��ƣ���д��ѧ����ʽ�����ݻ�ѧ����ʽ�ļ���
������������֤��ʵ��̽����Ҫ������ʵ����ʻ�仯���ɣ����ݸ�����ʵ����Ʒ���������ʵ�顢������̽������ͨ���۲졢��¼�ͷ�����ʵ����������֤�����ʵ����ʻ�仯���ɵȡ�

 ��ʦ������Ԫ��ĩ���100��ϵ�д�
��ʦ������Ԫ��ĩ���100��ϵ�д� ��У������Ԫͬ��ѵ��������ϵ�д�
��У������Ԫͬ��ѵ��������ϵ�д�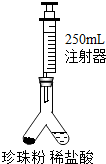 ��2013?������һģ��������������õ����յȹ�Ч�����������ϲ����������ʾ�������к�̼���80-93%��������4-14%��ˮ��2-4%��ʮ���ְ����ᡢ28����Ԫ�أ�Ȼ��һЩ���������û��յı��Ǽ��Ϲ�ҵ�������������Ƶ�ҩˮ������ϴ����ɹ�Ժ�ֱ�Ӽӹ����ۣ�����Ҫ�ɷ��ǣ�̼��ƣ������������������ƣ�������ij��ѧ��ȤС����Ʊ��������飬���ⶨ������̼��ƺ�����ʵ��̽��������
��2013?������һģ��������������õ����յȹ�Ч�����������ϲ����������ʾ�������к�̼���80-93%��������4-14%��ˮ��2-4%��ʮ���ְ����ᡢ28����Ԫ�أ�Ȼ��һЩ���������û��յı��Ǽ��Ϲ�ҵ�������������Ƶ�ҩˮ������ϴ����ɹ�Ժ�ֱ�Ӽӹ����ۣ�����Ҫ�ɷ��ǣ�̼��ƣ������������������ƣ�������ij��ѧ��ȤС����Ʊ��������飬���ⶨ������̼��ƺ�����ʵ��̽��������

 ����ֱ�����ˮ����ֽ��衢���ã��ⶨ�ϲ���Һ��pH����pH �� 7���>����<����=����Ϊ�����飬������ �� ��
����ֱ�����ˮ����ֽ��衢���ã��ⶨ�ϲ���Һ��pH����pH �� 7���>����<����=����Ϊ�����飬������ �� ��