题目内容
对比学习有利于发现事物的共性与个性。为探究酸的化学性质,同学们进行了如下实验。
| 实验内容 | 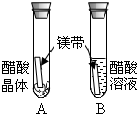 |  |  |
| 实验现象 | A试管内无明显现象,B试管中镁带表面观察到的现象是 。 | C、D两试管中均观察到有气泡产生。 | E试管中观察到的现象是 ; F试管中无明显现象。 |
| 结论 | 酸的很多反应通常在水溶液中才能完成。 | 不同的酸具有相似的化学性质。 | 不同的酸根会导致酸的“个性”有差异。 |
请分析上述现象并回答:
(1)不同的酸具有相似的化学性质,这是因为酸的组成中都含有 (填元素符号)。
(2)不同的酸根会导致酸的“个性”有差异,因此,可用 鉴别盐酸和硫酸。
(3)清洗试管时,将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀。废液缸里最终产生的白色沉淀中一定含有硫酸钡,该反应的化学方程式为 ,白色沉淀中可能还含有 (填化学式)。
有气泡产生或冒气泡 白色沉淀产生
(1)H(H+)
(2)氯化钡(氢氧化钡、硝酸钡、可溶性钡盐)
(3)Na2SO4+BaCl2→2NaCl +BaSO4↓ BaCO3
解析试题分析:醋酸属于酸,溶液中有氢离子,所以能与活泼金属反应,产生氢气,所以B试管中镁带表面观察到的现象是:有气泡产生或冒气泡;把BaCl2溶液滴加到稀硫酸中,发生反H2SO4+BaCl2=BaSO4↓+2HCl,有白色沉淀BaSO4生成
(1)不同的酸具有相似的化学性质,这是因为酸的组成中都含有H+
(2)不同的酸根会导致酸的“个性”有差异,硫酸中含有硫酸根,而盐酸不含有,所以可用氢氧化钡、氯化钡(可溶性钡盐)来鉴别盐酸和硫酸
(3)F试管中的无色液体含BaCl2和HCl,而C试管中的无色液体含的溶质有三种情况:1、只含Na2SO4,2、含Na2SO4和Na2CO3,3、含Na2SO4和H2SO4,将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡,说明C试管中的无色液体含的溶质Na2SO4和Na2CO3,所以废液缸里最终产生的白色沉淀中一定含有硫酸钡,该反应的化学方程式为:Na2SO4+BaCl2→2NaCl +BaSO4↓,当然还可能发生反应:Na2CO3+BaCl2=BaCO3↓+2NaCl,所以白色沉淀中可能还含有BaCO3
考点:酸的通性及个性

 阅读快车系列答案
阅读快车系列答案下图装置可以完成多个简单实验,具有药品用量少、实验现象明显、尾气不外逸等优点。
(1)若甲中吸有浓氨水,乙中吸有无色酚酞溶液,将甲、乙中的液体同时挤出,一段时间后,观察到无色酚酞溶液变红,说明分子具有的性质是________。
(2)若甲中吸有水,乙中吸有稀硫酸,烧杯①中盛有用石蕊溶液染成紫色的干燥纸花,烧杯②中盛有碳酸钠粉末。为了验证使石蕊变色的物质是碳酸而不是二氧化碳,应采取的实验操作是_______ _ 。
(3)若先将甲中的液体挤出,观察到气球明显鼓起,一段时间后恢复原状;再将乙中的液体挤出,气球又明显鼓起。请将下表中的试剂补充完整。
| | 滴管甲 | 烧杯① | 滴管乙 | 烧杯② |
| 试剂 | H2O | | | Mg |
分类法是学习化学的重要思想方法,依据同类物质性质的相似性,可以帮助我们做到举一反三。现有下列三组物质:
A.空气、胆矾、冰水、蔗糖
B.KOH、H2SO4、Ca(OH)2、Ba(OH)2
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白
| 组 别 | A组 | B组 | C组 |
| 分类标准 | 纯净物 | 碱 | |
| 不属于上述分类标准的物质 | 空气 | | SO2 |
(2)请仿照检验CO2的反应,写出SO2与石灰水的反应方程式 。
(3)下列各组物质间均能反应,写出③、④反应的化学方程式.。
①硫酸铜溶液和氢氧化钠溶液 ②碳酸钠溶液与硫酸
③氢氧化钠溶液与盐酸 。
④硝酸银溶液和氯化锌溶液 。
(4)NaOH溶液与CuSO4溶液能够反应,实质是因为它们在水中解离出来的OH-和Cu2+结合生成了Cu(OH)2沉淀。结合发生复分解反应的条件,请回答:Na2CO3溶液与H2SO4溶液能够反应的实质是它们在水中解离出 离子结合生成 。
许多植物的果实和花瓣中含有色素。现提取几种植物的果实或花瓣的汁液,用稀酸、稀碱和水逐一检验,现象记录如下表。
| 植物的汁液 | 在酸性溶液中 | 在水中 | 在碱性溶液中 |
| 牵牛花 | 红色 | 紫色 | 蓝色 |
| 万寿菊 | 黄色 | 黄色 | 黄色 |
| 胡萝卜 | 橙色 | 橙色 | 橙色 |
| 玫瑰 | 浅红色 | 浅红色 | 绿色 |
(1)上述植物的汁液不能用来区别稀酸和稀碱溶液的是 、 。(填植物的名称)
(2)手工制作一朵纸玫瑰花,用pH=12的某种溶液浸泡后晾干,用所提取的玫瑰的汁液均匀地涂在纸玫瑰花上,纸花会变成 色。
(3)与实验中常用的指示剂石蕊的变色原理相似的是 。(填植物的名称)