题目内容
下图是氢氧化钙的溶解度曲线图.现有10℃含l00g水的澄清氢氧化钙饱和溶液.若把该溶液用水浴加热到60℃(水的蒸发忽略不汁).下列说法错误的是( )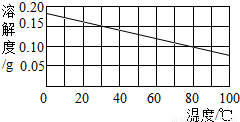
A.溶液变浑浊
B.溶液变为不饱和
C.溶液仍饱和
D.溶质质量分数变小
【答案】分析:根据固体物质的溶解度曲线可以判断该物质的溶解度随温度变化的变化情况,从而可以得出通过升温还是降温的方法使它的饱和溶液和不饱和溶液间相互转化,从而判断溶液中溶质的质量分数的变化.
解答:解:由于氢氧化钙的溶解度随温度的升高而减小,因此给它的饱和溶液升温时,它的饱和溶液中就会有晶体析出,因此溶液中就会出现浑浊,随着晶体的析出,溶液中溶质的质量分数就会越来越小,但溶液仍为饱和溶液.
故选B
点评:本题难度不大,主要考查了氢氧化钙的溶解度曲线,及根据溶解度曲线解决相关的问题,从而加深学生对固体溶解度的理解.
解答:解:由于氢氧化钙的溶解度随温度的升高而减小,因此给它的饱和溶液升温时,它的饱和溶液中就会有晶体析出,因此溶液中就会出现浑浊,随着晶体的析出,溶液中溶质的质量分数就会越来越小,但溶液仍为饱和溶液.
故选B
点评:本题难度不大,主要考查了氢氧化钙的溶解度曲线,及根据溶解度曲线解决相关的问题,从而加深学生对固体溶解度的理解.

练习册系列答案
相关题目
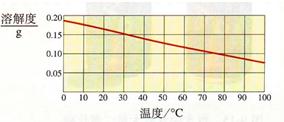 22、熟石灰的溶解度如下图所示.某同学在30℃时用固体熟石灰配制了饱和澄清石灰水溶液.取少量溶液于试管中,滴加酚酞试剂,溶液变红色.
22、熟石灰的溶解度如下图所示.某同学在30℃时用固体熟石灰配制了饱和澄清石灰水溶液.取少量溶液于试管中,滴加酚酞试剂,溶液变红色.
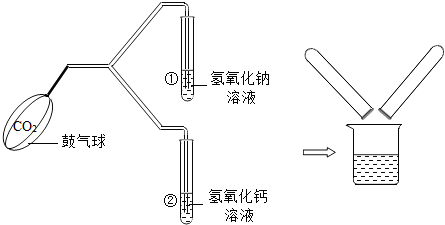 (2012?朝阳区一模)在化学实验技能考试中,有一题目是鉴别氢氧化钙溶液和氢氧化钠溶液,某同学进行了如下图所示的实验.
(2012?朝阳区一模)在化学实验技能考试中,有一题目是鉴别氢氧化钙溶液和氢氧化钠溶液,某同学进行了如下图所示的实验.