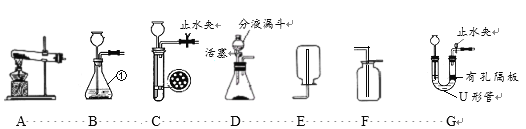
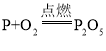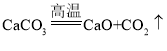题目内容
【题目】一氧化碳具有还原性,可将金属氧化物还原成金属,一氧化碳还原氧化铁的化学方程式为_____。课堂上老师给同学们一包黑色粉末,可能由铁粉和氧化铜粉末组成。为了确定该粉末的成分,同学们进行了如下探究实验,请回答下列有关问题。
(猜想假设)猜想1:黑色粉末是铁粉。 猜想2:黑色粉末是氧化铜粉末。 猜想3:_____。
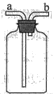
(实验验证)取少量黑色粉末,放入硬质玻璃管中,通入一氧化碳气体,片刻后加热充分反应(实验装置如图所示,夹持装置已略)。
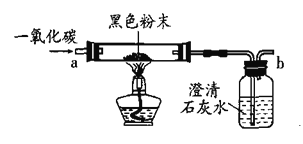
(实验分析)经过分析实验现象,得出黑色粉末为铁粉和氧化铜的混合物,实验中观察到的现象是_____。
(拓展反思)
(1)实验完毕后,先停止加热,继续通入一氧化碳直至玻璃管冷却至室温。继续通入一氧化碳的目的是_____。
(2)从环保角度上看,上图设计有不足之处,改进措施是_____。
(3)取该黑色粉末4g放入硬质玻璃管中,完全反应后称量硬质玻璃管内剩余固体的质量为mg,则m的取值范围是_____。
【答案】 铁粉和氧化铜粉末 黑色粉末部分变红,澄清石灰水变浑浊 防止生成的铜再次被氧化,防止澄清石灰水倒吸入玻璃管中 在b处放燃着的酒精灯(或安装尾气处理装置或在b处导管绑一个小气球)
铁粉和氧化铜粉末 黑色粉末部分变红,澄清石灰水变浑浊 防止生成的铜再次被氧化,防止澄清石灰水倒吸入玻璃管中 在b处放燃着的酒精灯(或安装尾气处理装置或在b处导管绑一个小气球) ![]()
【解析】
一氧化碳和氧化铁高温生成铁和二氧化碳,一氧化碳和氧化铜高温生成铜和二氧化碳,铜和氧气加热生成氧化铜。
一氧化碳和氧化铁高温生成铁和二氧化碳,故一氧化碳还原氧化铁的化学方程式为 。
。
[猜想假设]
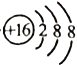
铁粉和氧化铜均是黑色粉末,可能含有其中一种或两种都有,故猜想1:黑色粉末是铁粉。猜想2:黑色粉末是氧化铜粉末。猜想3:铁粉和氧化铜粉末。
[实验分析]
一氧化碳和氧化铜高温生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊,故实验中观察到的现象是黑色粉末部分变红,澄清石灰水变浑浊。
[拓展反思]
(1)铜和氧气加热生成氧化铜,为防止铜再次被氧化,实验完毕后,先停止加热,继续通入一氧化碳直至玻璃管冷却至室温,此外继续通一氧化碳还可以防止澄清石灰水倒吸入玻璃管中。
(2)一氧化碳有毒,需要除去,从环保角度上看,不足之处的改进措施是在b处放燃着的酒精灯(或安装尾气处理装置或在b处导管绑一个小气球)。
(3)假设4g黑色粉末全部为氧化铜
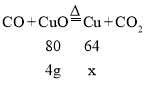
![]()
![]()
粉末是铁和氧化铁的混合物,则m的取值范围是![]() 。
。

【题目】如表是 NaCl、NH4Cl 在不同温度时的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | |
(1)以上两种物质的溶解度受温度影响较大的是_____。
(2)40℃时,将 40.6g NaCl 加入到 100g 水中,充分搅拌使之溶解,所得溶液的质量为_____g。
(3)20℃时,NaCl 饱和溶液的溶质质量分数为(精确到小数点后 1 位)_____。