��Ŀ����
����Ԫ������������У��Լ�������Ľ������ź���Ҫ�����ã���ش��������⡣
��1�������ӹ���ķ�����Һ�к���2��5%��NaNO2������һ�ֻ�����Ⱦ�������NH4Cl��Һ�������˷�����Һ��ʹNaNO2ת��Ϊ�����ʡ��÷�Ӧ���������У�
��һ����NaNO2+NH4Cl=NH4NO2+X
�ڶ�����NH4NO2=N2��+2H2O
�ٵ�һ����Ӧ��X�Ļ�ѧʽ�� ��
��NH4NO2�е����⡢������Ԫ�ص��������� �����е�Ԫ�صĻ��ϼ۷ֱ��� �� ��
��2����ͼ��һյ�Ͼ�̨�ƣ�ijʵ��С���ͬѧ���������й۲������������ʵ�顣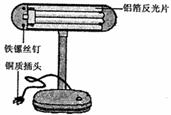
��С������̨�Ƶ�����˿�������Ѿ���ʴ��ԭ������������е� �ȷ����˻�ѧ��Ӧ��
��С�췢����������Ƭ������ɫ�����⼣��ԭ������������һ�����ܵ�����Ĥ�����ɸ�����Ĥ�Ļ�ѧ����ʽΪ ��
���ҹ��Ŵ���¯��ʯ��ZnCO3������ͭ��Cu2O����ľ̿�ۻ�Ϻ���ȵ�Լ800�棬�õ�һ������ƽ��ӵĺϽ𣬸úϽ����Ҫ�ɷ�Ϊ ����д����ͭ���ɵĻ�ѧ����ʽ ��
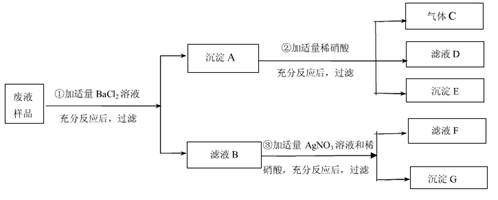
��3���ý������Ʊ�����ˮ��������������ˮ��K2FeO4���������£���ش��������⣺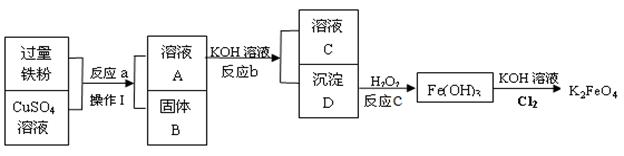
�ٹ���B�ijɷ��� ����Ӧa�Ļ�ѧ����ʽΪ: ��
�ڲ���I�������� ������I����Ҫ����������Ʒ������̨�������������Լ��� ����һ��ʵ����Ʒ���ƣ���
�۷�Ӧa��b��c��û���漰���Ļ�ѧ��Ӧ������ ������ĸ���ţ���
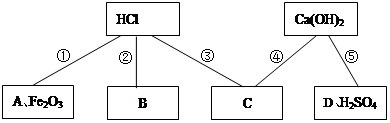
| A�����Ϸ�Ӧ | B���ֽⷴӦ | C���û���Ӧ | D�����ֽⷴӦ |
��1���� NaCl �� 7:1:8 -3 +3
��2���� ������ˮ��������O2��H2O�� �� 4Al+3O2 =2Al2O3
�� ͭ��п����Cu��Zn�� C + 2Cu2O 4Cu +CO2��
4Cu +CO2��
��3���� Cu��Fe��������Ҳ�ɣ� Fe + CuSO4 =" Cu" + FeSO4 �� ���ˡ���ֽ �� B
���������������1�������������غ㶨����ȷ�����ʵĻ�ѧʽ���ڵ�һ����Ӧ�У�NaNO2+NH4Cl�TNH4NO2+X����Ӧǰ��ԭ�ӡ���ԭ�ӡ���ԭ�ӡ���ԭ�ӡ���ԭ�ӵĸ����ֱ�Ϊ1��2��2��4��1����Ӧ��ԭ�ӡ���ԭ�ӡ���ԭ�ӵĸ����ֱ�Ϊ2��2��4����X�к���һ����ԭ�Ӻ�һ����ԭ�ӣ����X�Ļ�ѧʽ��NaCl��
�ڻ������и�Ԫ��������=��Ԫ�ص����ԭ��������ԭ�Ӹ���֮�ȣ����NH4NO2�е����⡢������Ԫ�ص��������ǣ���14��2������4��1������16��2��=7��1��8�����ݳ���Ԫ�صĻ��ϼۼ��������л��ϼ۴�����Ϊ���ԭ����з�����֪��NH4NO2��NH4��NԪ�صĻ��ϼ�Ϊ-3�ۺ�NO2��NԪ�صĻ��ϼ�Ϊ+3�ۣ�
��2�������ڿ�������ʴ��ʵ���������������е�������ˮ��ͬ���õĽ����̨�Ƶ�����˿�������Ѿ���ʴ��ԭ������������е�������ˮ���������˻�ѧ��Ӧ��
�ڳ����£����ڿ�������������Ӧ��������������Ĥ����Ӧ�Ļ�ѧ����ʽΪ��4Al+3O2�T2Al2O3��
����Ϊľ̿����Ҫ�ɷ���̼�����л�ԭ�ԣ����Կ��Խ�ZnCO3�ֽ������ZnO����ͭ��Cu2O����ԭ�õ�ͭ��п���ʺϽ����Ҫ�ɷ�Ϊͭ��п������ͭ�Ļ�ѧ����ʽΪ��C + 2Cu2O 4Cu +CO2����
4Cu +CO2����
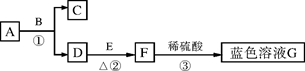
��3�����ɷ�Ӧ�����̿�֪������������������ͭ��Ӧ������������������ͭ�������ǹ����ģ��ڹ��˺�õ��Ĺ���B��Cu��Fe�Ļ�����Ӧa�Ļ�ѧ����ʽΪFe+CuSO4�TFeSO4+Cu��
����������Ӧa�õ��ǹ�Һ�Ļ���Ҫ����Һ�ֿ���Ӧ���еIJ����ǹ��ˣ�����ʱ��Ҫ����������Ʒ������̨�������������Լ�����ֽ��
���ɷ�Ӧ�����̿�֪����Ӧa��Fe+CuSO4�TFeSO4+Cu����һ�ֵ��ʺͻ����ﷴӦ��������һ�ֵ��ʺͻ���������û���Ӧ����Ӧb��FeSO4+2KOH=Fe��OH��2��+K2SO4���÷�Ӧ�������ֻ�����������ɷ������������µĻ�������ڸ��ֽⷴӦ����Ӧc��2Fe��OH��2+H2O2=2Fe��OH��3������������������һ�����ʣ����ڻ��Ϸ�Ӧ���ۺ�������Ӧ�����Ϳ�֪��û���漰�ķ�Ӧ�����ǷֽⷴӦ�����ԣ�ӦѡB


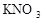 ��
��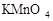 ��
��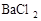 ��
��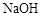 �е�һ�ֻ��֡�
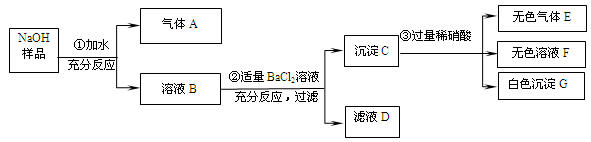
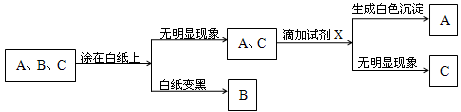
�е�һ�ֻ��֡�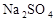 ��Һ��������ɫ���������Һ��һ�������е�������______________�����ܺ��е�������_______________��
��Һ��������ɫ���������Һ��һ�������е�������______________�����ܺ��е�������_______________��