题目内容
【题目】N(NO2)3是科学家近年发现的一种新型火箭燃料。下列关于N(NO2)3说法正确的是( )
A. N(NO2)3的相对分子质量为150
B. N(NO2)3中氮元素与氧元素的质量比是7:12
C. N(NO2)3中总共有3个N原子和6个O原子
D. N(NO2)3中氮元素的质量分数为![]() ×100%
×100%
【答案】B
【解析】
A、N(NO2)3的相相对分子质量=14×4+16×6=152,故错误;
B、N(NO2)3中氮元素和氧元素的质量比为(14×4):(16×2×3)=7:12,故正确;
C、N(NO2)3是由分子构成的,而不是由原子直接构成的,每个N(NO2)3分子中含有4个N原子和6个O原子,故错误;
D、N(NO2)3中氮元素的质量分数为![]() ×100%,故错误。
×100%,故错误。
故选B。

【题目】人类的生产生活离不开金属材料。
(1)人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”,在“五金”顺序中把金属_____的位置移到最后,正好符合由弱到强活动性顺序。
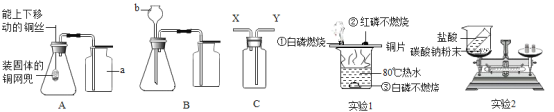
(2)铝、铁、铜是我们生产生活中使用比较广泛的金属。如图所示用品中,主要利用金属的延展性的是_____(填字母序号)。

(3)合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。一般来说,合金的熔点低于任何一种组成金属的熔点。下表是一些金属的熔点数据。
金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
保险丝由铋、铅、锡、镉组成,其熔点约为_____。
A.15~30℃; B.60~80℃; C.235~250℃; D.300~320℃。
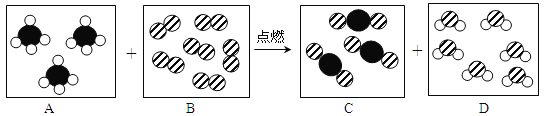
【题目】为了探究金属活动性,同学们将锌和铜分别放入稀硫酸中,锌的表面有气泡产生而铜不反应,写出锌和稀硫酸反应的化学方程式:_____。
老师告诉同学,铜和浓硫酸在加热的条件下也能反应且产生气体。
(提出问题)铜与浓硫酸反应的生成物是什么?其中气体是什么?
(猜想假设)同学们对产生的气体作出了猜想。
猜想一:氢气;
猜想二:二氧化硫;
猜想三:氢气和二氧化硫的混合气体。
同学们作出以上猜想的依据是_____。
(査阅资料)(1)二氧化硫有刺激性气味,会污染空气;
(2)二氧化硫可以使品红溶液褪色,能被氢氧化钾溶液吸收;
(3)浓硫酸具有吸水性,可以干燥气体。
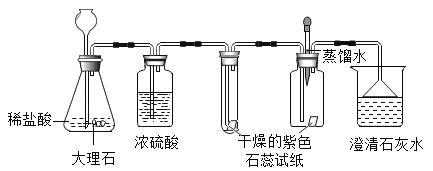
(实验探究)师生设计了如下装置进行实验(部分仪器省略),请完成下列表格。
主要实验步骤 | 主要现象 | 解释或结论 |
①加热装置A一段时间 | 装置B中的现象是_____ | 有二氧化硫生成 |
②点燃装置D处酒精灯 | 装置D玻璃管中无明显现象 | 猜想_____正确 |
③停止加热,将铜丝上提,向装置A中玻璃管鼓入空气 | ||
④冷却,观察A中溶液颜色 | A中液体变为_____色 | 有硫酸铜生成 |
(表达交流)
(1)在步骤③中,鼓入空气的目的是_____。
(2)铜与浓硫酸反应的化学方程式为:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+_____。
CuSO4+SO2↑+_____。
(反思拓展)
若将装置A中铜丝换成锌片,随着反应的进行,硫酸的浓度逐渐变小,装置D玻璃管中看到的现象是_____。